近日,湘雅科研团队取得了多项突破。敲黑板!一起看看2026年1月的科研成果吧~
以下成果根据湘雅各二级学院、附属医院官网等整理。
湘雅医院急诊科护理团队在国际著名期刊发表原创研究论文
唐北沙、沈璐团队发表系列神经元核内包涵体病(NIID)原创性研究成果
胡硕团队和冯莉团队合作在《Science Advances》与《Advanced Science》期刊连续发表原创研究成果
谢辉团队在国际期刊集中发布多项原创成果
易文君团队在国际期刊发表论文揭示靶向IL27RA 重塑免疫微环境
彭道泉团队研究结果揭示创新药ANGPTL3抗体可使纯合子家族性高胆固醇血症患者LDL-C显著降低
湘雅二医院心血管外科团队在新型小口径血管移植物研究领域取得创新突破
李霞、赵斌课题组发文揭示1型糖尿病缓解期关键免疫互作机制
吴忠仕团队在国际知名期刊发表高水平论文提出血管分层修饰策略
周后德团队研发出MetsObesity肥胖分型法
肖扬团队揭示Galectin-3介导Treg细胞功能障碍驱动1型糖尿病,靶向抑制剂TD139展现治疗新潜力
张晶晶、贺洁宇团队在《Ageing Research Reviews》发表人工智能在老年糖尿病领域的应用综述
周建大团队在Molecular Cancer发表原创论著 揭示circROR1驱动黑色素瘤转移新机制
梁德生等首次揭示先天性肾上腺皮质增生症遗传图谱,实现基因筛查
刘静团队揭示红细胞生成调控新机制
湘雅医院急诊科护理团队在国际著名期刊发表原创研究论文
近日,湘雅医院护理团队在国际外科学顶尖期刊《International Journal of Surgery》(国际外科学杂志)(IF=10.3,JCR Q1区)发表题为《Mapping the Knowledge Landscape: A Bibliometric Analysis of Gut Microbiota in Cancer Immunotherapy with Implications for Clinical Translation》(绘制知识图谱:癌症免疫治疗中肠道微生物群的文献计量分析及其临床转化意义)的原创性研究论文。急诊科副主任护师苏盼为论文独立第一作者。

该研究采用文献计量学方法,首次系统绘制了肠道菌群在癌症免疫治疗领域的知识发展图谱,揭示了该领域从“萌芽-发展-爆发”的三阶段演进路径,识别出五大研究热点:免疫检查点抑制剂、乳腺癌、结直肠癌、疗效评价及肿瘤微环境,并构建了“菌群-免疫-肿瘤”三角知识框架。研究进一步指出,抗生素使用、粪便菌群移植等临床干预手段与免疫治疗效果密切相关,为肿瘤患者(尤其是围手术期)的个体化治疗与综合管理提供了重要理论依据。
此项成果体现了护理人员从临床实践出发、深入参与前沿医学交叉研究的专业能力与学术影响力。论文的发表,为未来肿瘤免疫治疗的个性化策略优化与围手术期管理提供了科学支持,彰显了湘雅护理人不断探索、推动临床转化研究的担当与实力。
文章链接:https://doi.org/10.1097/JS9.0000000000004476
唐北沙、沈璐团队发表系列神经元核内包涵体病(NIID)原创性研究成果
近日,中南大学湘雅医院唐北沙/沈璐团队在《Nature Communications》(IF=15.7)、《eBioMedicine》(IF=10.8)等国际知名期刊发表多篇NIID相关原创性研究,不仅揭示了潜在的疾病进展生物标志物,更在基因治疗等前沿干预策略上开展了临床前研究,为最终实现NIID的精准诊断与有效治疗奠定了坚实基础。
沈璐团队在Lancet子刊《eBioMedicine》上以论著形式在线发表了题为《Plasma p-tau species are elevated in presymptomatic and symptomatic neuronal intranuclear inclusion disease》的原创性研究成果,揭示了NIID存在tau病理改变,扩展了tau蛋白谱系疾病。该研究纳入NIID患者和症状前个体2个队列,通过对多队列人群的外周血生物标志物分析,发现NIID患者中p-tau217、p-tau231、p-tau181、α-syn、NfL及GFAP等多种生物标志物水平显著升高,其中p-tau217能有效区分NIID患者与健康对照,但难以鉴别NIID与阿尔茨海默病(AD),提示两者在tau病理上可能存在重叠。

唐北沙/刘琼团队与暨南大学李晓江、李世华团队合作,在《Nature Communications》上以论著形式在线发表了题为“Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease”的原创性研究成果,首次成功实现了对NIID致病突变的精准切除和修复。该研究运用CRISPR/Cas9基因编辑系统,靶向GGC重复序列侧翼特定区域,通过双sgRNA协同作用成功实现了对NOTCH2NLC基因GGC重复序列的高效、特异性切除,并通过同源定向修复技术将其校正至生理正常长度。该编辑策略的有效性、特异性及安全性,在患者来源的IPSC、NPC及转基因小鼠模型中得到了系统性验证,为后续临床转化奠定了坚实基础。

胡硕团队和冯莉团队合作在《Science Advances》与《Advanced Science》期刊连续发表原创研究成果
近日,中南大学湘雅医院核医学科胡硕教授团队联合神经内科冯莉教授团队,在颞叶癫痫精准影像与发病机制研究领域取得系列原创性进展,相关成果连续发表于《Science Advances》(中科院一区Top期刊,IF = 12.5)和《Advanced Science》(中科院一区Top期刊,IF = 14.1)。研究围绕新型分子影像探针的临床应用、癫痫关键病理机制解析及潜在治疗靶点探索展开,为颞叶癫痫的精准评估和靶向干预提供了新的研究证据。
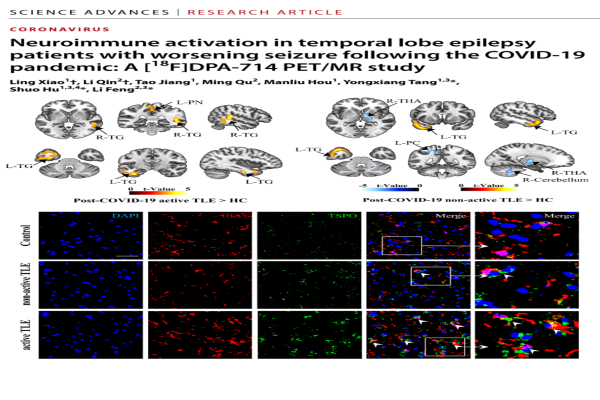
在发表于《Science Advances》的研究中(题为Neuroimmune activation in temporal lobe epilepsy patients with worsening seizure following the COVID-19 pandemic: A [18F]DPA-714 PET/MR study),研究团队综合分子影像、血液生物标志物及组织学证据,在同一癫痫队列中系统描绘了新冠感染后癫痫发作加重患者所伴随的“中枢-外周”双重免疫激活特征。研究结果提示,神经免疫反应可能与“新冠后活动性颞叶癫痫”的发生进展密切相关。将血浆炎症因子检测与TSPO PET成像联合应用,有望为癫痫相关神经炎症的评估、动态监测及免疫干预疗效评价提供新的分子影像与生物标志物联合检测手段。
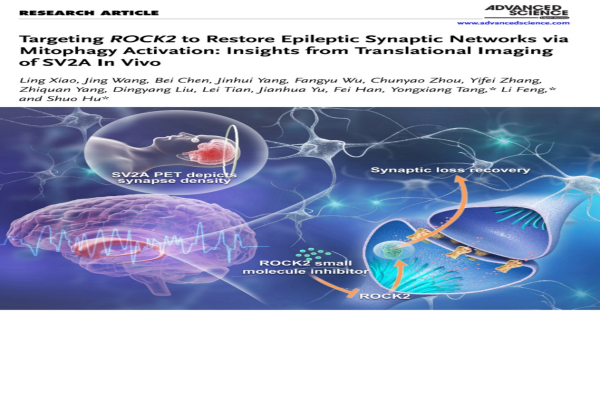
另一项发表于《Advanced Science》的研究(题为Targeting ROCK2 to restore epileptic synaptic networks via mitophagy activation: insights from translational imaging of SV2A in vivo)聚焦颞叶癫痫突触网络重塑及其靶向干预机制。研究团队利用靶向SV2A的[18F]SynVesT-1 PET成像,刻画了颞叶癫痫患者突触网络的异常重塑特征。结合PET成像与转录组学分析,研究进一步鉴定了突触网络重塑的关键调控基因ROCK2。动物实验结果提示,ROCK2抑制剂可通过激活线粒体自噬,改善突触密度和突触网络效率,并降低癫痫发作强度与频率,改善认知功能。该研究为颞叶癫痫突触层面的机制解析及靶向治疗策略提供了重要实验依据。
谢辉团队在国际期刊集中发布多项原创成果
近期,湘雅医院运动系统损伤修复研究中心及埃米医学湖南省重点实验室谢辉教授团队,在《自然·衰老》《肠道微生物》《先进科学》等六本国际期刊集中发表系列原创成果,涵盖骨骼衰老、哮喘、代谢性血管疾病、耐药菌感染与肿瘤治疗等方向。
一、揭秘“脑-骨轴”:大脑远程调控骨衰老的全新机制
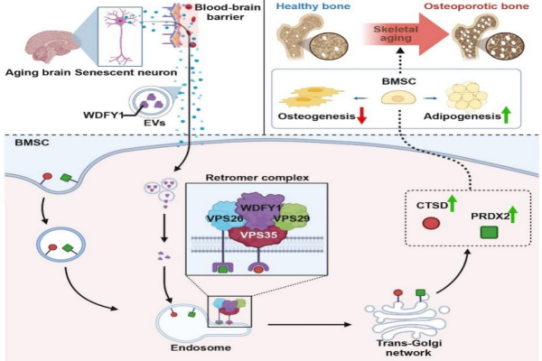
发表于《自然·衰老》(IF=19.5)的研究,促使我们对骨衰老仅由局部调控的传统认知进行重新审视。团队成员陈春媛副研究员(骨科)、饶珊珊副研究员(骨科)等,发现衰老大脑海马及皮层神经元可通过分泌囊泡,将WDFY1蛋白“远程输送”至骨骼,诱导骨髓脂毒性,促进骨质疏松进展。该研究不仅揭示了骨衰老的中枢调控新机制,也为骨质疏松诊治提供了潜在新靶点。
二、构建“肠-骨-肺轴”:跨界揭示哮喘炎症新通路
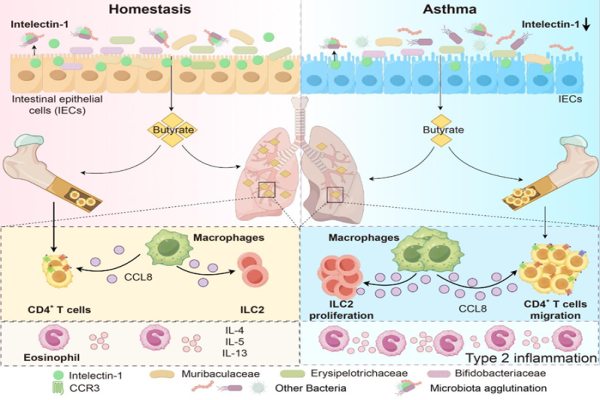
在《肠道微生物》(IF=11.0)发表的研究中,团队成员、呼吸与危重症医学科何诗月博士、胡新月助理研究员、潘频华教授,骨科王振兴副研究员等,融合呼吸、消化与骨代谢学科视角,提出创新性的“肠-骨-肺轴”调控模式。研究阐明了哮喘状态下肠道功能变化如何影响菌群,进而通过骨髓免疫细胞加剧肺部炎症的完整链条,为哮喘的全身性干预提供了全新理论依据和治疗靶点。
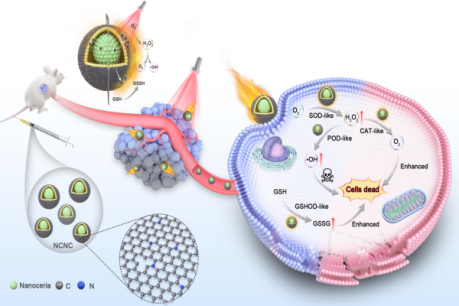
三、发现“肝-血管对话”:揭示代谢性肝病促血管钙化新机制
发表于《先进科学》(IF=14.1)的研究,聚焦代谢性脂肪肝病与血管钙化的临床关联。团队成员与曾召林博士(内分泌专业)、刘江华教授(内分泌科)、祖旭宇教授(肿瘤学科)合作,跨界探索发现,病变肝脏分泌的特异性囊泡可作为信使,直接促进动脉粥样硬化与钙化进程。这一发现深化了对器官间“远程病理通讯”的理解,为防治相关血管并发症开辟了新方向。
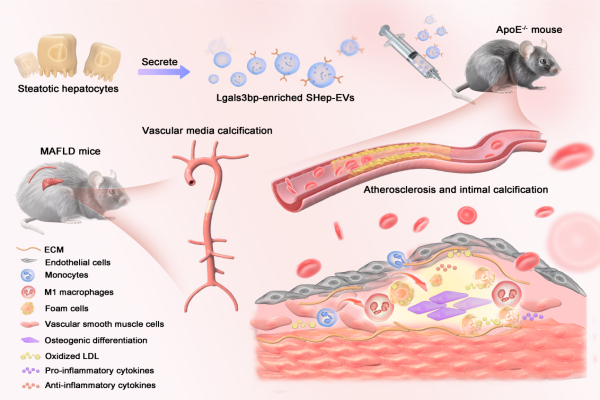
四、揭秘“肠-血管轴”:揭示间歇性禁食通过益生菌蛋白改善血管钙化新路径
发表于《纳米生物技术杂志》(IF=12.6)的研究,深入探讨了饮食干预对心血管健康的保护新机制。团队成员与曾诗雨博士生(内分泌)、刘江华教授(内分泌科)合作研究发现间歇性禁食诱导的肠道益生菌分泌蛋白B2URF3可作为关键信使,有效抑制血管平滑肌细胞成骨转分化并缓解血管钙化进程。这一发现不仅阐明了全新的“肠-血管轴”远程调控机制,也为血管钙化的临床干预提供了潜在的生物标志物和新型治疗靶点。
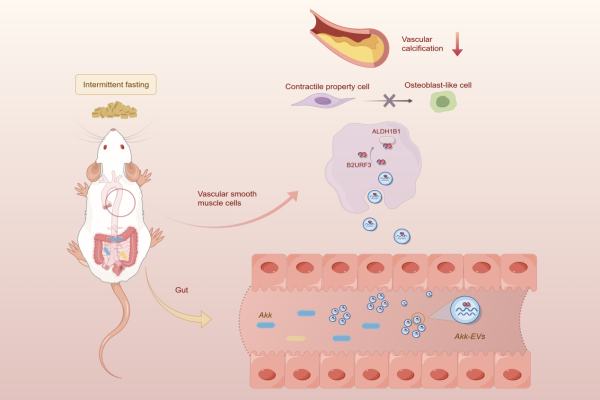
五、设计压电催化材料:协同攻克耐药性骨髓炎难题
面对耐药菌感染性骨髓炎的临床困境,团队成员吴阳博士后(生物材料专业)、陈贝博士(骨科)、王振兴副研究员(骨科)、唐举玉教授(骨科)等,在《生物活性材料》》(IF=20.3)发表的研究中,融合材料科学、微生物学与骨科学,创新性设计出一种智能纳米颗粒。该材料在超声触发下,能同时实现穿透生物膜、高效杀菌和促进骨再生三重功能,展示了学科交叉协同攻坚复杂疾病的强大潜力。
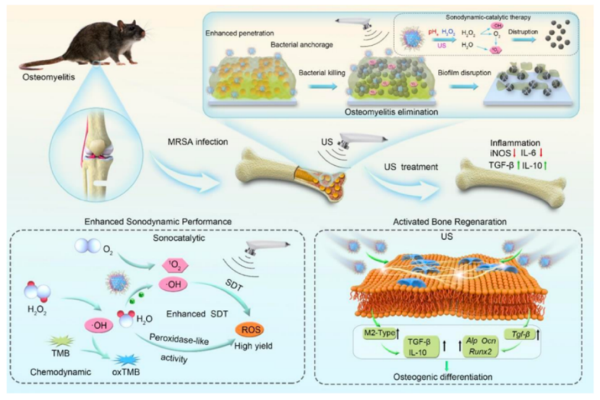
六、创新“链甲”纳米酶:实现肿瘤催化治疗的精准调控
发表于《先进医疗材料》(IF=9.6)的研究,针对肿瘤催化治疗的选择性难题,团队成员刘宏基助理研究员(材料物理与化学专业)等与王辉研究员(中国科学院合肥物质科学研究院强磁场实验室)合作,借鉴材料学“空间限域”理念,设计出具有核壳结构的纳米酶。该催化剂能在近红外激光精准激活下,于肿瘤部位高效产生治疗物质,同时保护正常组织,显著提升了治疗的安全性,展现了纳米酶技术的临床转化前景。
易文君团队在国际期刊发表论文揭示靶向IL27RA 重塑免疫微环境
近日,中南大学湘雅二医院乳腺外科易文君教授团队在《先进科学》(Advanced Science,IF=14.1,中科院一区TOP期刊)发表题为 “靶向 IL27RA 通过调控肿瘤细胞及肿瘤微环境增强三阴性乳腺癌免疫治疗效果”(Targeting IL27RA Enhances Immunotherapy in Triple-Negative Breast Cancer by Modulating Tumor Cells and the Tumor Microenvironment)的原创性研究论文。

三阴性乳腺癌(TNBC)因其侵袭性强、复发风险高、可靶向治疗选择有限,是乳腺癌精准治疗领域的难点之一。近年来,免疫检查点抑制剂(ICB)联合化疗逐步应用于TNBC新辅助治疗,相关临床研究表明,该联合方案可使病理完全缓解率(pCR)较单纯化疗提高约10%–20%。然而,仍有相当比例患者难以从免疫治疗中获得显著获益。因此,如何识别耐受/不敏感人群并进一步提升疗效,是当前亟需解决的重要问题。
在此背景下,研究团队对接受新辅助免疫治疗联合化疗的患者样本进行了单细胞转录组分析。研究表明,IL27RA通过激活PI3K/AKT信号通路,下调MHC-I并抑制抗原呈递相关基因表达,从而削弱CD8⁺ T细胞介导的肿瘤杀伤效应。考虑到免疫治疗效应依赖肿瘤微环境,研究团队进一步构建Il27ra全身敲除小鼠并开展单细胞分析,结果显示系统性Il27ra缺失可重塑免疫生态:CD8⁺ T细胞趋化/炎症特征增强,NK细胞向更成熟、细胞毒性更强的谱系分化,整体支持“抑制IL27RA可增强PD-1阻断治疗敏感性”的结论。
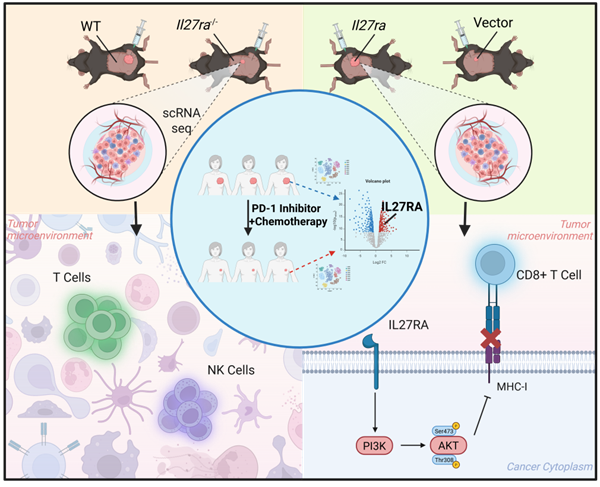
研究进一步指出,高IL27RA/低MHC-I 表型的患者亚群可能具有更高风险或更强免疫逃逸倾向,或可从“IL27RA抑制 + PD-1/PD-L1阻断”的联合策略中获益。此外,研究也提出了与PI3K/AKT通路抑制剂(如Alpelisib)或免疫激动策略协同增强抗肿瘤效应的可能性,并强调未来需通过更精准的递送与干预方式,尽可能降低系统性免疫扰动带来的潜在风险。
彭道泉团队研究结果揭示创新药ANGPTL3抗体可使纯合子家族性高胆固醇血症患者LDL-C显著降低
近日,中南大学湘雅二医院心血管内科彭道泉教授团队在《美国医学会心脏病学》(JAMA Cardiology,IF= 14.1,中科院一区TOP期刊)发表题为“抗ANGPTL3抗体SHR-1918治疗纯合子型家族性高胆固醇血症一项II期临床试验“的原创性研究论文。

纯合子家族性高胆固醇血症(HoFH)是一种罕见且危及生命的遗传性疾病。患者自出生起低密度脂蛋白胆固醇(LDL-C)水平即极度升高,表现为皮肤黄色瘤和早发冠心病,有报道此类患者最早5岁可发生心肌梗死和猝死。HoFH患者低密度脂蛋白受体(LDLR)功能通常缺失或严重受损,传统降脂药(如他汀)和近年兴起的PCSK9抑制剂的疗效差,以往只能依赖肝脏移植和血液透析降低其胆固醇。最新的研究发现靶向血管生成素样蛋白3(ANGPTL3)可通过不依赖LDLR的途径降低HoFH血脂水平。
在此背景下,研究团队评估了新药SHR-1918——一种靶向ANGPTL3的全人源单克隆抗体,在接受稳定背景降脂治疗仍控制不佳的成人HoFH患者中的疗效与安全性。受试者接受SHR-1918,600 mg Q4W 皮下注射,持续12周,随后进入8周随访期。研究期间的背景降脂治疗保持不变。
本研究共纳入26例HoFH患者,患者平均年龄为(36.1±12.2)岁。基线LDL-C水平为433.59±173.74 mg/dL(11.23±4.50 mmol/L);甘油三酯(TG)中位数为87.61 mg/dL(0.99 mmol/L)。治疗12周后,LDL-C水平较基线降低59.09%,TG水平较基线降低48.91%。不同基因型的LDL-C水平均显著降低,第12周时复合杂合子、纯合子以及双杂合子的LDL-C水平较基线分别降低56.40%、61.32%及72.21%。15.4%的患者实现了LDL-C达标。研究期间,无严重不良事件报道。
本项II期研究显示,每4周一次皮下注射SHR-1918可为HoFH患者带来显著且持续的LDL-C降低(平均60%降幅),明显减轻皮肤黄色瘤,并具有良好的安全性及耐受性。其疗效和给药方式相较于国际上获批HoFH适应症的ANGPTL3单抗Evinacumab(需静脉输注,LDL-C降幅平均49%左右)更有效和更方便,有望为HoFH患者提供一种高效、便捷的新型治疗选择。
湘雅二医院心血管外科团队在新型小口径血管移植物研究领域取得创新突破
近日,湘雅二医院心血管外科、心血管用生物工程材料湖南省工程实验室吴忠仕教授团队,在国际化学工程领域期刊《化学工程杂志》(Chemical Engineering Journal,中科院一区,IF: 13.2)上发表了题为《互穿层次化两性离子水凝胶促进去细胞化小口径血管移植物再生》(Interpenetrated hierarchical polyzwitterionic hydrogels promote decellularized small-diameter vascular grafts regeneration)的原创性研究论文。该研究创新性地将仿生两性离子水凝胶与去细胞牛肋间动脉相结合,成功开发出一种具备修复功能的新型小口径血管移植物。该移植物在植入大鼠体内6周后通畅率达到100%,且成功实现了血管内皮与平滑肌的再生。

冠状动脉搭桥手术是治疗严重冠心病的重要手段,而近半数患者因自身血管条件不佳,面临无合适血管可用的困境。现有小口径人工血管极易发生血栓堵塞和内膜增生,长期通畅率不理想。研发性能优良、易于获取的小口径人工血管一直是心血管用材料研究领域的难题。
针对该研究挑战,湘雅二医院心血管外科吴忠仕教授团队以去细胞处理的牛肋间动脉为天然支架,开展分区功能化设计:血管内表面形成致密光滑的水凝胶涂层,有效抑制血小板粘附与血栓形成;血管中膜与外膜的水凝胶以10–20微米的互通多孔结构为宿主细胞浸润、营养物质传输和新生血管长入提供关键的“生命通道”。该血管移植物在大鼠腹主动脉移植模型中表现出卓越性能:植入后不仅全部通畅、无狭窄迹象,超声检测显示其血流速度与自体血管相当;且组织学分析证实血管壁结构完整,并伴有良好的组织整合与再生。
此研究的关键创新在于将两性离子水凝胶前驱液渗透至血管支架内部,通过光固化技术,在血管壁内“原位构建”出具有层次化结构的水凝胶网络,通过精巧的物理结构设计,充分调动机体自身的修复潜能。该研究为小口径血管移植物的临床转化提供了新的思路。研究获得了湖南省重大科技专项的支持,是湘雅二医院心血管外科坚持以临床问题导向,深耕心血管组织工程与再生医学领域取得的又一重要成果。目前,研究团队正积极推进大动物实验,争取早日实现临床转化,为广大心血管疾病患者带来新希望。
李霞、赵斌课题组发文揭示1型糖尿病缓解期关键免疫互作机制
近日,中南大学湘雅二医院内分泌与代谢性疾病国家临床医学研究中心李霞教授与赵斌教授团队在代谢领域权威期刊《自然·代谢》(Nature Metabolism,IF=20.8)发表研究论文《IL-21介导的T细胞与NK细胞在1型糖尿病缓解期的相互作用机制》(IL-21 mediates crosstalk between T cells and NK cells during the remission of type 1 diabetes),揭示了1型糖尿病缓解期关键免疫互作机制。
1型糖尿病(T1D)是一种以T细胞介导胰岛β细胞破坏为主要病理基础的自身免疫疾病。临床上,部分新发T1D患者在起病后可进入短暂的缓解期(“蜜月期”):此阶段残余β细胞功能部分恢复,血糖控制改善,外源胰岛素需求下降。然而,该阶段的启动与维持机制仍未完全阐明,亦缺乏可有效诱导或延长蜜月期的干预手段,已成为T1D免疫治疗与精准干预亟待突破的关键瓶颈。
在团队前期发现致病性T细胞新亚群并阐明其介导1型糖尿病(T1D)进展与缓解机制的研究基础上,本研究进一步将视角拓展至先天免疫系统,系统解析了 CD161⁺CD4⁺ T细胞–IL-21–CD226⁺ NK细胞轴在T1D缓解过程中的关键作用。研究首次提出“辅助性T细胞—自然杀伤细胞轴向互作”的免疫调控模式,为深入理解T1D发病机制及探索靶向干预策略提供了新的思路与理论依据。
研究基于多组T1D临床样本,综合采用单细胞转录组测序、流式免疫表型分析与体外功能实验,并结合NOD小鼠模型开展多维度体内干预,系统解析了“CD161⁺CD4⁺ T细胞–IL-21–CD226⁺ NK细胞” 这一关键免疫互作轴在T1D缓解期中的调控机制。研究发现,在T1D进展期, CD226⁺ NK细胞亚群显著扩增,呈现转录活性增强、葡萄糖代谢上调及细胞毒性增强等高度激活特征;而在缓解期,该亚群比例明显下降。与此同时,研究鉴定 CD161⁺CD4⁺ T细胞是IL-21的重要来源,其频率在缓解期同样降低,并与CD226⁺ NK细胞活化程度呈显著正相关。
进一步的体外研究表明,IL-21可通过激活PI3K–AKT–mTOR信号通路,增强CD226⁺ NK细胞的细胞毒性功能;在体内层面,小鼠实验进一步证实,阻断该互作轴的多个关键环节,包括使用 IL-21敲除(KO)小鼠、IL-21R Fc融合蛋白、mTOR抑制剂雷帕霉素或抗CD226单抗,均可有效延缓糖尿病发生,减少胰岛内CD226⁺ NK细胞浸润并缓解局部炎症反应。
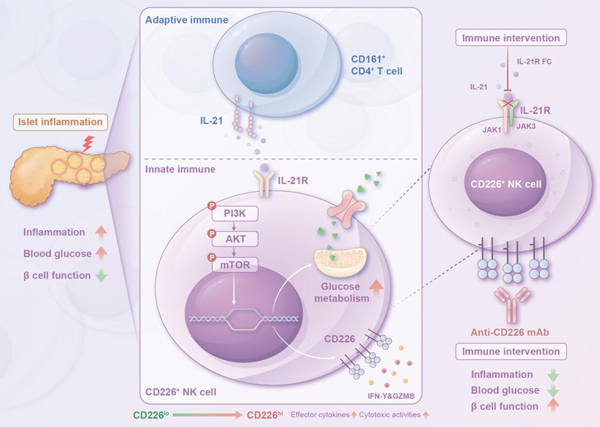
本研究首次从“适应性免疫—先天免疫”协同调控的角度,揭示了T1D缓解期(“蜜月期”)免疫稳态重塑与耐受重建的关键机制,进一步加深了对蜜月期免疫学本质的认识。更为重要的是,研究明确了可干预的关键节点,为延长乃至人工诱导T1D缓解期提供了新的理论依据与潜在治疗靶点,具有明确的临床转化价值。
吴忠仕团队在国际知名期刊发表高水平论文提出血管分层修饰策略
近日,中南大学湘雅二医院心血管外科、心血管用生物工程材料湖南省工程实验室吴忠仕教授团队在国际生物材料领域顶级期刊《生物材料》(Biomaterials)(IF=12.9)发表原创性研究论文《基于中空介孔二氧化硅纳米粒的VEGF/IL-4时空程序化控释系统增强脱细胞血管移植物内皮化及免疫介导的基质重塑》(Spatiotemporally Programmed VEGF/IL-4 Delivery via HMSNs Enhances Endothelialization and Immune-Mediated Matrix Remodeling in Acellular Vascular Grafts)。

心血管疾病是全球致死致残的首要原因,冠状动脉疾病、先天性心脏病等常需小口径血管移植物进行血管重建,而人口老龄化和代谢性疾病高发进一步加剧了临床需求。现有小口径人工血管面临内皮化进程缓慢和血管基质重塑不足两大瓶颈,难以匹配人体血管的生理功能,传统单一因子干预或普通递送系统也无法满足血管分层再生的复杂需求。
针对这一挑战,吴忠仕教授团队提出了“内膜靶向再生+外膜时序释放”的血管分层修饰策略,该策略能精准调控纳米颗粒尺寸,实现了生物活性因子的高效负载及分区时序性释放。关键创新在于将空间分区设计与时序释放策略相结合,首次在小口径血管移植物中实现“募集-分化-重塑”的全程调控。使用该策略的移植物植入体内后3个月形成了全层的细胞及较完整的三层血管结构,植入后6个月全部通畅,无动脉瘤形成,表现出卓越的体内性能。这一突破为构建具备长期通畅与结构稳定性的原位再生型小口径血管移植物提供了新的设计范式。
周后德团队研发出MetsObesity肥胖分型法
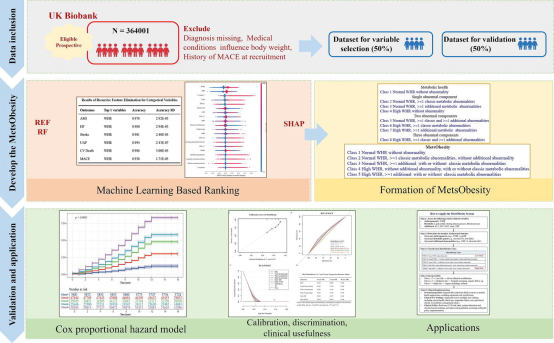
近日,中南大学湘雅二医院周后德教授课题组创新性地提出了MetsObesity—— 一种全新的风险分型系统,用于更准确地预测肥胖及代谢异常人群的长期心血管疾病风险。该研究成果已在线发表于 Journal of Advanced Research(影响因子 13,CiteScore 22.1),为全球肥胖相关心血管疾病预防提供了全新解决方案。
MetsObesity 是全球首个将体脂分布与代谢指标、炎症状态及肝脏相关指标相结合的综合风险评估系统,用于预测未来15年心脑血管疾病风险。与传统评估工具不同,MetsObesity 仅纳入可干预的危险因素,这些因素可通过生活方式调整、药物治疗和规范医疗加以改善,具备极强的临床实用性。该系统综合考虑三大类核心指标,均为临床常规检查项目,无需额外增加检测成本,主要包括:体型与脂肪分布指标;经典代谢健康指标:包括血压、空腹血糖、血脂;新型关键关联指标:以往常被忽视的炎症水平(如 C反应蛋白)、肝酶及尿酸,这些指标与代谢紊乱和血管损伤密切相关。依托上述指标,MetsObesity将个体清晰划分为五个风险等级,从低风险到极高风险,便于临床医生快速风险评估。
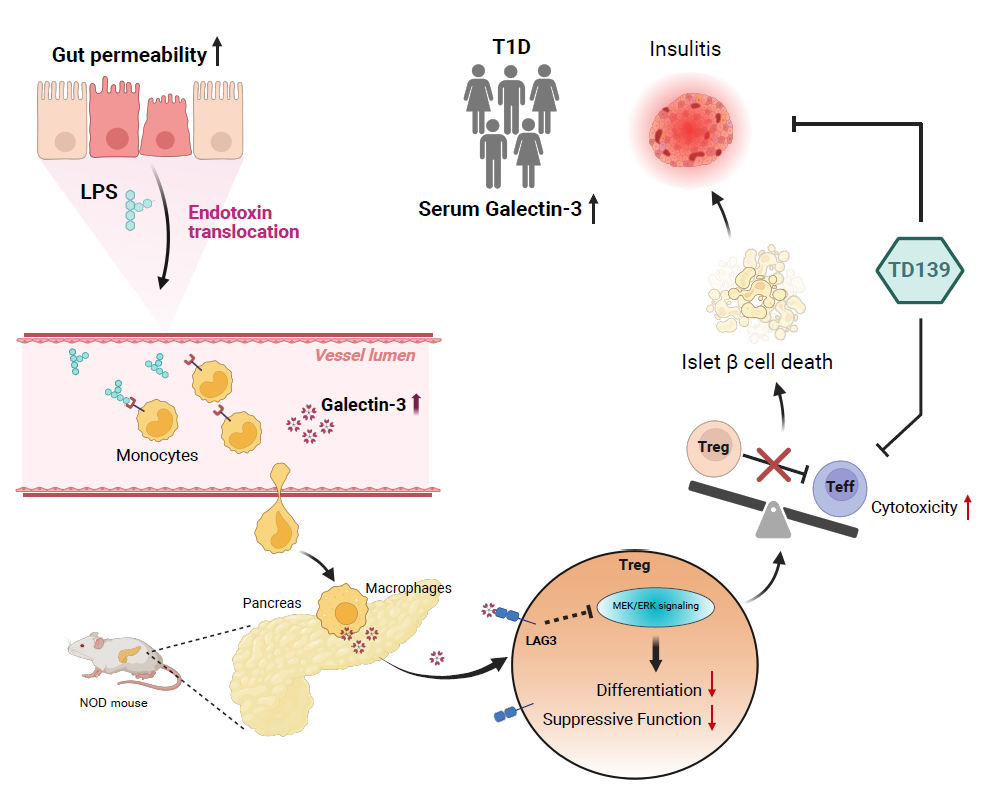
肖扬团队揭示Galectin-3介导Treg细胞功能障碍驱动1型糖尿病,靶向抑制剂TD139展现治疗新潜力
近日,中南大学湘雅二医院肖扬教授团队在《Science Advances》(IF:12.5)上在线发表了题为Galectin-3 exacerbates autoimmune diabetes by limiting regulatory T cell differentiation and function的研究论文。该研究揭示了T1D“肠漏”引起的低内毒素血症刺激单核/巨噬细胞产生并分泌经典炎症相关凝集素 Galectin-3,其通过限制Treg细胞分化并削弱其抑制功能,进而放大胰岛局部免疫失衡,而基因敲除或药理抑制Galectin-3均能缓解NOD小鼠(T1D自发模型)胰岛炎并降低糖尿病发生。
该研究系统阐明Galectin-3损害Treg细胞分化与免疫抑制功能的致病机制,完整揭示从肠道环境启动到T细胞功能失调的病理链条,更重要的是,研究通过基因敲除与药理抑制双重证据验证,将Galectin-3确立为靶向Treg干预T1D进程的可行策略,为后续临床转化奠定扎实基础。
原文链接:https://doi.org/10.1126/sciadv.adz7916
张晶晶、贺洁宇团队在《Ageing Research Reviews》发表人工智能在老年糖尿病领域的应用综述
近日,中南大学湘雅二医院张晶晶、贺洁宇课题组在老年医学领域权威期刊《Ageing Research Reviews》(老年医学领域TOP 3,IF 12.4)发表综述论文,题为“Applications of AI in the management of elderly diabetes patients” 。该论文研究了AI在老年糖尿病管理中的创新应用,系统整理了AI技术在老年糖尿病疾病筛查、诊断监测、治疗干预等全阶段的研究进展,为解决老年糖尿病患者管理问题提供了全新思路与科学支撑。

老年糖尿病患者群体日益庞大,全球65岁以上人群患病率已超20%,且常伴随跌倒、肌肉减少症、认知障碍、抑郁等老年综合征。同时,传统诊疗模式存在侵入性强、实时监测不足、患者依从性低等局限。该论文为针对性破解这些难题,全面阐释了AI技术如何通过机器学习、深度学习等算法,结合可穿戴设备、高通量技术、智能设备等构建非侵入式、个性化、智能高效的老年糖尿病管理体系。论文指出,AI在老年糖尿病管理中展现出极高价值:在血糖调控领域,AI驱动的连续血糖监测系统、预测模型及人工胰腺技术,实现了血糖的实时追踪与精准胰岛素输注;针对糖尿病视网膜病变、肾病、大血管病变、糖尿病足等并发症,AI算法可高效分析影像、生化指标,有助于早期筛查与风险预判;针对老年患者常见的抑郁、衰弱、跌倒等共病与老年综合征,AI通过可穿戴设备监测、行为数据分析等方式,提供了系统的评估与干预方案。此外,论文还深入探讨了AI在临床应用中的数据质量、公平性、伦理规范等关键问题,为技术转化临床实践提供了重要参考。
原文链接:
https://www.sciencedirect.com/science/article/abs/pii/S156816372500306X?dgcid=author
周建大团队在Molecular Cancer发表原创论著 揭示circROR1驱动黑色素瘤转移新机制
近日,中南大学湘雅三医院烧伤整形科周建大团队在国际肿瘤领域权威期刊《Molecular Cancer》(分子癌症,中科院一区,IF=33.9)发表原创性论著“CircROR1 binds HNRNPL to regulate FOXO4 pre-mRNA splicing, promoting cutaneous melanoma metastasis and serving as a therapeutic target via RNAi-loaded PEG-LNPs”(环状RNA ROR1通过与HNRNPL结合调控FOXO4前体mRNA剪接,进而促进皮肤黑色素瘤转移,并可通过负载RNAi的PEG-LNPs作为治疗靶点)。该研究在国际上首次揭示了CircROR1通过结合剪接因子HNRNPL重塑FOXO4前体mRNA可变剪接,从而驱动皮肤黑色素瘤(cutaneous melanoma, CM)转移进展的关键分子机制,并进一步验证靶向circROR1的RNA干扰(RNAi)纳米药物的策略,为转移性黑色素瘤的精准治疗提供了新的潜在靶点和转化路径。

梁德生等首次揭示先天性肾上腺皮质增生症遗传图谱,实现基因筛查
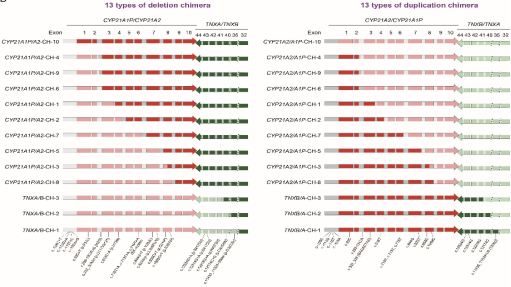
近日,生命科学学院医学遗传学研究中心联合国内11家区域性医学遗传中心,应用单分子长读长测序技术,系统解析了先天性肾上腺皮质增生症(CAH)的遗传图谱,并开展了大规模的一线新生儿筛查。研究成果以“基于长读长测序对21,239名新生儿队列进行先天性肾上腺皮质增生症的遗传特征分析与筛查”为题,发表在国际顶级医学遗传学期刊《Genome Medicine》(IF:11.2,中科院大类一区)。
本研究首次提供了基于(中国)人群的完整CAH变异谱、以及CAH和NCCAH致病变异携带率和发病率,为精准防控提供了基础数据。一线并行筛查结果显示,新生儿CAH生化筛查阳性预测值仅为0.94%(1/106),漏筛了全部NCCAH。相比之下,LRS准确识别出全部经典CAH和NCCAH,没有假阳性结果。由于LRS技术能够一次性精准检测CAH相关基因的全部变异,可以缩短病因诊断周期,实现“筛诊一体”。另外,本研究首次攻克了NCCAH因症状隐匿而导致的临床诊断与分型难题,使得在新生儿期或症状出现前早期识别NCCAH高危个体成为可能,为实现早期干预、改善长期预后,以及开展精准的遗传咨询和携带者筛查提供了关键依据。
刘静团队揭示红细胞生成调控新机制
近日,中南大学生命科学学院刘静教授团队在红细胞生成(erythropoiesis)精细调控机制研究方面取得系列重要进展,成果发表于高水平SCI期刊《Nucleic Acids Research》(IF=13.1)。

研究团队发现染色质重塑因子HLTF可直接结合GATA1启动子并促进其转录表达。体内外模型证实,HLTF缺失导致GATA1显著下调,进而抑制细胞增殖、诱导凋亡并阻滞红系分化。多组学联合分析显示,HLTF缺失引起红系基因启动子区域染色质可及性降低,并削弱GATA1全基因组结合能力。值得注意的是,HLTF不仅作为GATA1的上游调控因子,还可与GATA1相互作用,招募TAL1、BRG1等协同调控;同时GATA1反向激活HLTF表达,二者形成正反馈调节环路,共同维持红系分化相关转录程序的稳定性。临床数据分析进一步揭示,HLTF在真性红细胞增多症(PV)等疾病中显著失调,提示其或为红系疾病的潜在分子标志物与治疗靶点。




