近日,湘雅科研团队取得了多项突破。敲黑板!一起看看2026年2月的科研成果吧~
以下成果根据湘雅各二级学院、附属医院官网等整理。
陈翔、肖易团队在《The Lancet》发表全球皮肤疾病谱变迁研究
湘雅医院联合湘雅药学院在《iMeta》杂志发表治疗炎症性肠病新成果
朱红团队发表高水平综述系统阐述癌症甲基化精准诊治新策略
李源课题组构建膀胱癌铜死亡纳米治疗新策略
金鑫团队发表糖尿病性勃起功能障碍发病机制及干预新策略原创性研究成果
刘军团队最新研究成果揭示显式推理机制在放射学诊断中的作用
向大雄、吴军勇团队系列研究取得突破,揭示炎症治疗与肿瘤免疫新策略
刘姗姗团队发现肺泡巨噬细胞外泌体调控肺泡再生新机制
方芳、姜文敏团队发表眼科本科教学方法新突破
王冰课题组发表了基于壳聚糖的复合支架作为生物活性锶递送系统介导加速骨再生的研究成果
蔡娟、董政团队揭示SUMO修饰稳定IκBα保护脓毒症相关急性肾损伤的新机制
王明团队系统阐释TET/5hmC表观遗传轴在胶质瘤中的作用,为精准治疗提供新思路
刘军团队最新研究成果揭示显式推理机制在放射学诊断中的作用
肖嵘团队揭示S-硫巯基化修饰调控系统性硬化症纤维化新机制
王龙教授团队在高水平期刊《International Journal of Surgery》发表重要研究成果
余正课题组在《Nature Microbiology》发表肠道微生物氨调控肠道神经与动力的原创性研究成果
张永昌团队在发表“非小细胞肺癌免疫化疗给药时间的随机三期试验”的临床研究成果
倪千喜团队“一种混合AI策略在自动化放疗计划中的应用研究”的研究成果
王静团队发表“呋喹替尼联合信迪利单抗治疗错配修复功能完整型晚期子宫内膜癌的多中心、单臂Ib/II期临床试验”的研究成果
于晓晖团队联合程岩团队发表“基于结构导向PROTAC策略靶向降解eEF2K治疗三阴性乳腺癌”的研究成果
周慧俊团队发表“多功能荧光探针用于同时检测Cys、Hcy和超氧阴离子:揭示其在肿瘤氧化应激与铁死亡中的潜在应用”的研究成果
陈翔、肖易团队在《The Lancet》发表全球皮肤疾病谱变迁研究
近日,中南大学湘雅医院陈翔教授、肖易副教授团队联合麻省总医院Esther E. Freeman教授、伦敦卫生与热带医学院Sinéad M. Langan教授领衔的团队在《The Lancet》上发表论文,系统分析了全球皮肤疾病谱的变迁规律,着力回答皮肤健康领域未来迫切需要回答的三个重大问题。

《The Lancet》借此契机宣布成立首个皮肤健康委员会,该委员会由中南大学湘雅医院牵头,联合全球多个大洲的皮肤病学、疾病负担、流行病学及实施科学等多领域的学者与专家共同开展,是全球皮肤健康领域率先开展的高层次学术行动。
委员会将聚焦三大核心领域:探究各地区及生命全周期中皮肤病的可预防、可干预负担及关键驱动因素;为加速皮肤健康领域全民健康覆盖设定可量化目标并探索实施模式,涵盖社区健康教育、初级保健服务整合等方面;明确全球核心皮肤健康服务基本包内容,涉及预防、诊断、药物可及性等多个关键领域。委员会将借助不同区域典型案例,阐明重点挑战与应对策略,提供差异化实施路径。同时深入探究四个关键问题,包括分析工业化等因素对皮肤疾病谱的影响;绘制全球皮肤科人力资源分布图谱,梳理强化服务能力的新兴策略;揭示面临双重皮肤病负担国家的困境与挑战;探索借助人工智能等技术创新,改善黑素瘤等皮肤肿瘤的及时发现与管理。委员会未来将发布综合报告与政策指南,开展多地区学术活动及部长级圆桌会议,并与世界卫生组织等伙伴及全球患者紧密协作,推动科学、医学、政策协同,助力全民皮肤健康覆盖。
湘雅医院联合湘雅药学院在《iMeta》杂志发表治疗炎症性肠病新成果
近日,中南大学湘雅医院药学部黄琼教授、老年外科吴畏教授,联合中南大学湘雅药学院艾可龙教授团队在炎症性肠病(IBD)治疗领域取得重要进展,相关研究成果在国际权威学术期刊《iMeta》(《整合宏组学》,IF=33.2)在线发表,为临床IBD及其合并艰难梭菌感染(IBD-CDI)的诊断治疗提供了创新性解决方向,具备重大临床转化价值。
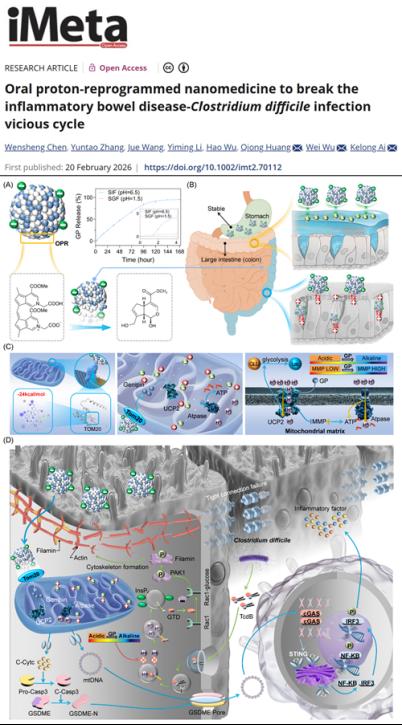
炎症性肠病(IBD)全球患病率持续攀升,目前已影响全球约700万患者。IBD患者易发生多种病原体共感染,其中艰难梭菌感染(CDI)占比高达97%,且合并CDI的IBD患者预后更差、病情更易恶化。艰难梭菌毒素B(TcdB)会破坏肠上皮细胞(IECs)间的紧密连接,损伤肠道屏障功能,进而加剧“IBD-CDI”恶性循环,推动病情进展。当前,临床治疗IBD-CDI的主要方案为抗生素与一线IBD治疗药物联用,但该方案存在药物治疗冲突、毒性效应叠加的高风险,临床应用受限。
针对这一临床痛点,黄琼、吴畏、艾可龙教授团队通过生物信息学分析、体内外实验验证及临床标本检测,首次发现解偶联蛋白2(UCP2)在IBD患者肠上皮细胞中高度表达,且会诱导线粒体功能障碍;进一步研究证实,UCP2诱导的线粒体损伤会促进肠上皮细胞酸化,加重艰难梭菌毒素B(TcdB)的毒性作用。基于这一核心发现,团队成功设计并开发出一种新型口服纳米药物OPR,该药物可依序靶向肠道病变部位、线粒体及UCP2,精准破解IBD-CDI临床治疗难题。
OPR采用“IBD病灶-肠上皮细胞(IECs)线粒体”序贯靶向药物释放系统构建,通过将甘氨酸与京尼平(GP,一种强效UCP2抑制剂)聚合,形成粒径为5-10纳米的纳米颗粒。口服给药后,OPR可在胃部高酸性环境中保持结构稳定,进入IBD病灶的弱酸性环境后,能缓慢释放活性成分GP,释放时长可达6天;同时,带负电荷的OPR可特异性靶向带正电荷的IBD结肠炎症区域,避开带负电荷的健康肠段,实现精准靶向给药,降低药物对正常组织的损伤。
在小鼠IBD模型实验中,OPR展现出优异的治疗效果,不仅能有效减轻肠上皮细胞焦亡,还可抑制巨噬细胞cGAS-STING通路激活,其疗效显著优于5-氨基水杨酸、地塞米松、JAK1抑制剂乌帕替尼、TNF-α单克隆抗体英夫利西单抗等一线临床治疗药物。此外,OPR还可通过代谢重编程降低肠上皮细胞乳酸水平、抑制细胞酸化,从而提高肠上皮细胞对TcdB的耐受性,有效缓解IBD-CDI并发症。该研究从“抑制肠上皮细胞焦亡+提升细胞毒素耐受性”的双重角度,为IBD-CDI综合征治疗提供了全新范式。
朱红团队发表高水平综述系统阐述癌症甲基化精准诊治新策略
近日,中南大学湘雅医院肿瘤学教研室、肿瘤放疗科朱红教授团队在国际知名学术期刊《Experimental Hematology & Oncology(实验血液学与肿瘤学)》(JCR Q1,IF: 13.5)上发表了题为“Targeting epigenetic methylation: emerging diagnosis and therapeutic strategies in cancer”(靶向表观遗传甲基化:癌症的新兴诊断及治疗策略)的重要综述论文。

该研究系统解析了甲基化在癌症早筛、耐药机制及临床治疗中的重要作用。
1.破解表观遗传“生命代码”,揭示肿瘤演进新机制甲基化修饰作为表观遗传学的核心,在不改变DNA序列的前提下调节基因表达并维持基因组稳定性。朱红教授团队详细绘制了涵盖DNA、RNA及组蛋白修饰的甲基化“全景图”:
l DNA甲基化:通过在CpG岛甲基化促进癌基因激活或抑制抑癌基因表达,显著影响肿瘤的发生发展。
l RNA甲基化:以m6A修饰为核心,参与调控癌细胞增殖、迁移、代谢及治疗抗性的产生。
l组蛋白甲基化:主要发生在H3和H4的赖氨酸与精氨酸残基上,精确控制转录活性及DNA修复过程。
2. 精准医疗“新哨兵”:甲基化液体活检引领早筛革命早期诊断是提升癌症生存率、降低死亡率的关键。朱红教授团队指出,基于循环肿瘤DNA(ctDNA)甲基化模式的液体活检技术正成为极具潜力的非侵入性筛查手段。并提出将甲基化抑制剂与放化疗、靶向治疗、免疫疗法及饮食疗法的协同方案。为患者提供早期癌症筛查新方式、克服治疗抵抗的新手段以及制定个性化治疗的新策略。
原文链接:https://doi.org/10.1186/s40164-026-00760-w
李源课题组构建膀胱癌铜死亡纳米治疗新策略
近日,中南大学湘雅二医院李源教授课题组在国际一流学术期刊《Advanced Functional Materials》(中科院一区期刊,IF=19)上发表了题为“Mitochondria-Targeting Nanocuproptosis Breaks Immune Resistance”的原创性研究论文。李源教授团队长期致力于医工交叉相关研究,现已成功研发出一种新型纳米药物(MTPY-Cu@Alb),该药物可有效逆转膀胱癌的免疫抵抗现象,并增效膀胱癌化疗的治疗效果,有望为膀胱癌患者带来更多治疗方案。
原文链接:https://doi.org/10.1002/adfm.202528750

研究团队创新性地设计并合成了MTPY-Cu@Alb纳米颗粒系统,该系统能够通过精准靶向肿瘤线粒体,诱导肿瘤细胞发生铜死亡并激活免疫系统。这一发现为肿瘤免疫治疗提供了新思路,尤其是在免疫耐受和肿瘤转移的治疗中展现出巨大潜力。研究发现铜死亡不仅通过引发线粒体应激激活AMPK/mTOR通路调控CD276,还通过DLAT/c-MYC轴下调CD47,逆转了肿瘤细胞对免疫系统的逃逸。这一新机制的提出,填补了铜死亡在免疫耐受调节中的研究空白。通过优化铜递送系统,MTPY-Cu@Alb能够在极低剂量条件下显著下调CD276和CD47的表达,增强免疫细胞对肿瘤的识别和清除。该纳米系统不仅提高了铜死亡的诱导效率,还有效增强了T细胞和巨噬细胞的抗肿瘤功能。MTPY-Cu@Alb能够突破传统免疫检查点抑制,成功重塑肿瘤免疫微环境,显著抑制肿瘤的原发生长和转移,且在化疗后进一步增强抗肿瘤免疫反应。研究团队的这一新型纳米平台为肿瘤免疫治疗提供了一个低毒、高效的治疗策略,有望为临床肿瘤治疗开辟新路径。
金鑫团队发表糖尿病性勃起功能障碍发病机制及干预新策略原创性研究成果
近日,中南大学湘雅二医院金鑫教授团队在糖尿病性勃起功能障碍(Diabetes-mediated Erectile Dysfunction, DMED)发病机制及精准干预领域取得重要进展,相关成果发表在国际著名期刊《Nature Communications》(中科院一区Top期刊,IF=15.7)上。研究以“Fbp1介导海绵体乳酸蓄积在糖尿病性勃起功能障碍中的机制及干预研究”为题,系统揭示DMED中海绵体乳酸异常蓄积的分子机制,并提出基于Fbp1靶点的mRNA治疗新策略。

该研究纳入60例DMED患者及健康对照,证实DMED患者血清乳酸水平显著升高,且与勃起功能障碍程度相关。动物与细胞实验进一步发现,糖尿病环境下海绵体乳酸蓄积明显增加,可损害海绵体结构和平滑肌含量,抑制海绵体平滑肌细胞活性并促进其病理性表型转化。
机制研究表明,糖代谢关键酶Fbp1在维持海绵体代谢稳态中发挥核心作用。Fbp1功能缺失加重乳酸相关损伤,而过表达则具有保护效应。进一步研究发现,组蛋白甲基转移酶Suv39h1通过H3K9me3修饰抑制Fbp1转录;棕榈酰转移酶Zdhhc13介导Fbp1棕榈酰化修饰,影响其糖异生功能和乳酸生成,形成双重调控机制。
在转化探索方面,团队构建脂质纳米颗粒(LNP)包裹的Fbp1-C282S mRNA递送系统,实现海绵体靶向治疗,显著改善DMED小鼠勃起功能。
刘军团队最新研究成果揭示显式推理机制在放射学诊断中的作用
近日,中南大学湘雅二医院放射科主任刘军教授课题组在《数字医学》(npj Digital Medicine,影响因子15.1)发表了题为《通过大型推理模型对结论进行推理在放射学中的诊断与解释收益》(Diagnostic and interpretive gains from reasoning over conclusions with a large reasoning model in radiology)的研究性论文。

该研究创新性地对比了模型的“显式推理过程”与“单纯结论输出”,并与非推理模型(如GPT-4.5, DeepSeek-V3)进行了横向评测。研究发现,显式推理过程在诊断完整性上表现最优,显著减少了漏诊和误诊,特别是在识别易被忽视的继发性病变(Secondary Diagnoses)方面具有显著优势。相比于仅输出结论,推理过程在全面性、可解释性和无偏见性方面均获得了更高的评分。
针对模型错误原因的分析发现,存在“结论失败”(Concluding Failure)现象,即模型推理正确但最终结论错误的风险,强调了透明化推理在核查AI决策中的重要性。人机协同实验表明,显式推理能显著提升放射科医师(尤其是低年资医师)对信息完整性和推理逻辑的感知,尽管其冗长的输出在一定程度上增加了阅读时间成本。
这项工作证明了在放射学诊断中引入显式推理机制,能有效提升诊断的完整性与可解释性,为未来构建更加可信、透明的AI辅助诊断系统提供了新的评估范式与理论依据。
向大雄、吴军勇团队系列研究取得突破,揭示炎症治疗与肿瘤免疫新策略
近日,中南大学湘雅二医院药学部向大雄教授团队在三阴性乳腺癌(TNBC)生物疗法、急性胰腺炎(SAP)纳米药物治疗及胞外囊泡(EVs)临床转化领域取得多项创新突破。相关研究成果分别发表在国际权威学术期刊《Journal of Advanced Research》(中科院一区,IF:13)、《Journal of Controlled Release》(中科院一区,IF:11.5)以及《Materials Today Bio》(中科院一区,IF:10.2)上。这系列研究不仅深入探讨了重大疾病的病理机制,还成功验证了多种生物模拟及活性材料策略,为临床精准治疗提供了全新视角。
其中关于三阴性乳腺癌(TNBC)的研究发表在《Materials Today Bio》上。研究团队开发了一种名为A-SPB的非基因工程活性细菌反应器。该系统利用希瓦氏菌(SO)对缺氧肿瘤微环境的趋化性,通过主动耗竭半胱氨酸(Cysteine)来切断谷胱甘肽(GSH)合成路径,并产生硫化氢阻断代谢旁路,从而触发强效的肿瘤免疫原性铁死亡。此外,表面修饰的普鲁士蓝纳米粒子不仅增强了光热治疗效果,还充当了“生物开关”,在清除肿瘤的同时诱导细菌自裂解以确保生物安全性,并激活全身抗肿瘤免疫反应。

原文链接:https://doi.org/10.1016/j.mtbio.2026.102843
另一项重要成果发表在《Journal of Advanced Research》上。研究团队针对重症急性胰腺炎(SAP),设计并验证了一种名为FePTX@CM NPs的炎症驱动仿生纳米多酚递药系统。该系统表面包覆巨噬细胞膜,赋予其强大的胰腺病灶靶向能力。机制研究表明,其中的原花青素(PYD)通过抑制线粒体ROS/高尔基体应激来减少胰腺酶过量分泌,而己酮可可碱(PTX)则通过抑制Zbp1信号通路阻止巨噬细胞泛凋亡(PANoptosis)。这种双重调节策略显著缓解了炎症进展并减少了组织损伤,为SAP的临床管理提供了新方案。

原文链接:https://doi.org/10.1016/j.jare.2025.04.006
此外,研究团队在《Journal of Controlled Release》发表了一篇关于胞外囊泡(EVs)临床转化的综述。文章系统总结了EVs在存储过程中的稳定性挑战,详细讨论了冷冻保存、喷雾干燥和冻干技术对囊泡膜完整性及载荷稳定性的影响。针对诊断标志物、给药载体和直接疗法等不同应用场景,研究团队提出了基于新型材料(如水凝胶、微针阵列)的优化保存策略,旨在通过标准化、可扩展的保存方案加速胞外囊泡技术从实验室走向临床实践。

原文链接:https://doi.org/10.1016/j.jconrel.2026.114706
刘姗姗团队发现肺泡巨噬细胞外泌体调控肺泡再生新机制
近日,国家代谢性疾病临床医学研究中心、中南大学湘雅二医院刘姗姗教授团队在国际知名期刊《Journal of Nanobiotechnology》(IF=12.6)发表了题为“Extracellular vesicles from alveolar macrophages promotes pulmonary fibrosis through suppression of lung alveolar regeneration”的原创性论文。该研究揭示了巨噬细胞来源的细胞外囊泡(EVs)介导肺泡再生障碍,促进肺纤维化的具体机制,为开发新型治疗策略提供了重要靶点。
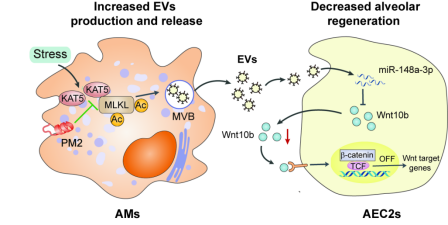
肺纤维化(PF)是一种进行性间质性肺病,其中特发性肺纤维化(IPF)恶性度最高,患者确诊后 3-5 年生存率极低。目前临床获批的抗纤维化药物仅能延缓病情,无法逆转病理损伤,核心原因是其发病机制尚未完全明确。肺泡上皮再生能力受损是肺纤维化发展的关键,肺泡 2 型上皮细胞(AEC2s)作为肺内干细胞,其自我更新和分化能力对肺泡修复至关重要,而肺泡巨噬细胞(AMs)与肺泡上皮细胞间的调控通讯机制此前尚未明确。该研究证实慢性肺损伤会通过上调乙酰转移酶KAT5,乙酰化MLKL蛋白,从而促进AMs大量产生并释放EVs。这些EVs被邻近的AEC2s摄取后,通过抑制Wnt10b的表达阻断了β-catenin信号通路,最终导致AEC2s自我更新及分化受阻,进而导致肺泡再生障碍,推动肺纤维化发生。基于这一全新发现的分子调控通路,研究团队进一步研发出靶向干扰 KAT5-MLKL 相互作用的多肽PM2。PM2阻断KAT5和MLKL相互作用后能显著抑制肺纤维化的进展。
该研究首次阐明了AMs与 AEC2s 之间通过 EVs 介导的细胞间通讯在肺纤维化中的关键作用,揭示了 KAT5-MLKL-EVs-miR-148a-3p-Wnt10b 这一全新的肺纤维化调控通路,同时研发的多肽PM2为肺纤维化的靶向治疗提供了全新的候选药物。这一发现不仅加深了对肺纤维化发病机制的理解,也为临床开发更有效的肺纤维化治疗药物奠定了基础。
方芳、姜文敏团队发表眼科本科教学方法新突破
近日,湘雅二医院眼科方芳、姜文敏在JMIR Medical education(JCR1区,IF:12.6)上发表“Combining Problem-Based Learning Methods With the WeChat Platform in Teaching Ophthalmology: Randomized Controlled Trial”文章。该研究以队列研究形式探讨了眼科本科教学(Problem based learning, PBL)联合中国特色的微信平台交流方法,与传统课堂教学的比较,对于眼科本科生教学质量与评估提供了创新方法与理论。中南大学湘雅二医院为论文的第一作者和通讯作者单位,姜文敏主任医师为论文的独立通讯作者,方芳副研究员为独立第一作者。

眼科学习对医学生来说具有独特的挑战,因为眼睛的解剖结构复杂,并且需要掌握必要的实践技能。基于问题的学习PBL是一种以学生为中心的方法,能够培养临床推理能力和自主学习能力。为了应对传统教学方法的时间和后勤限制,该研究实施了一种基于微信的PBL 模式,利用该平台的效率和互动性来增强学生对眼科的学习参与度和技能获取。
医学教育在本科教学中越来越多地融入创新策略,以更好地帮助学生为临床实践中的挑战做好准备。有效的教学方法对于充分准备学生进行临床实践和发展他们作为未来临床医生的胜任力至关重要。该研究针对传统眼科教育中面临的挑战,即被动学习阻碍了本科生临床技能和自信心的培养。研究旨在评估基于微信的PBL 方法在提升学生学习自我认知、主动性、组织能力、临床技能和知识掌握方面的有效性和可接受性。
王冰课题组发表了基于壳聚糖的复合支架作为生物活性锶递送系统介导加速骨再生的研究成果
近日,中南大学湘雅二医院脊柱外科王冰教授课题组在国际顶尖期刊《Carbohydrate Polymers》(自然指数期刊,中科院一区Top,IF:12.5)上发表了基于壳聚糖的复合支架作为生物活性锶递送系统介导加速骨再生的研究成果。课题组基于临床重大问题的探索及医工交叉研究,成功研发了一种新型的骨修复材料(CS/SF@SrAlg),这一创新成果为骨缺损修复提供了全新的治疗策略。

创伤、肿瘤切除或感染引起的骨缺损是骨科临床实践中重大的临床挑战。目前的骨移植物材料往往受到成骨能力差、供体来源有限以及机械性能不足的限制。在本研究中,我们利用微流控电喷雾和纤维碎裂重组技术,开发了一种由壳聚糖、丝素蛋白纤维和锶藻酸盐微球组成的复合骨再生支架(CS/SF@SrAlg)。这种基于壳聚糖的复合支架结合了优异的生物相容性、广泛的可获得性以及增强的机械性能。组分间的化学交联和物理相互作用促进了复合系统的形成,实现了Sr²⁺的可控释放。该支架具有多级多孔结构,促进细胞浸润,而丝素蛋白纤维则改善了机械完整性,并有助于维持有利的微环境。体外实验表明,该支架显著增强了细胞增殖、迁移和成骨矿化,细胞存活率达到120%。在大鼠颅骨缺损模型中,支架显著促进血管生成和成骨,在植入8周后观察到81.8%的骨再生覆盖率。此外,RNA转录组学分析揭示,它通过调控关键的PI3K-Akt信号通路发挥成骨作用。因此,CS/SF@SrAlg支架代表了一种用于骨缺损修复的有前景的生物材料策略,在临床应用方面具有巨大潜力。
论文全文链接:https://www.sciencedirect.com/science/article/abs/pii/S0144861726001980
蔡娟、董政团队揭示SUMO修饰稳定IκBα保护脓毒症相关急性肾损伤的新机制
近日,中南大学湘雅二医院肾内科蔡娟/董政团队在Molecular Therapy(中科院一区,IF: 12.0)上发表题为“SUMOylation protects against sepsis-associated acute kidney injury by stabilizing IκBα”的原创性研究论文。脓毒症相关急性肾损伤(sepsis-associated acute kidney injury , SA-AKI)是重症监护病房中常见的危重症,具有极高的死亡率,其病理机制涉及NF-κB信号通路的过度激活及其引发的炎症风暴。SUMO修饰是一种重要的蛋白质翻译后修饰形式,参与调控多种信号通路精细调控,但其在SA-AKI中的具体作用及调控机制尚属未知。IκBα是NF-κB信号通路关键的上游抑制蛋白,其稳定性对于抑制炎症风暴至关重要。
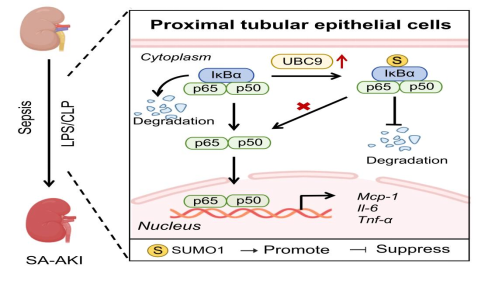
该研究主要发现在脂多糖LPS或盲肠结扎穿孔(CLP)诱导的SA-AKI小鼠模型中,SUMO修饰唯一的E2连接酶泛素结合酶9 (ubiquitin-conjugating enzyme 9 , UBC9) 显著上调。特异性敲除肾近端小管中的Ubc9或用药物抑制SUMO修饰,均会加剧肾脏炎症反应和损伤。机制研究证实,SUMO修饰在脓毒症应激下作为一种内源性保护机制被激活,促进了IκBα上特异赖氨酸位点的SUMO修饰,从而阻止泛素蛋白酶体介导的降解,通过稳定IκBα蛋白来有效阻断NF-κB信号的过度激活。该研究首次揭示了SUMO修饰在SA-AKI中的保护性角色及其分子机制,为临床防治SA-AKI提供了新的潜在治疗策略。
王明团队系统阐释TET/5hmC表观遗传轴在胶质瘤中的作用,为精准治疗提供新思路
近日,中南大学湘雅二医院神经外科王明团队在国际期刊《Pharmacological Research》(IF:10.5)发表题为“The TET/5hmC mediated epigenetic landscape in glioma: From molecular mechanisms to therapeutic targeting and future perspectives”的综述文章。该文围绕胶质瘤中TET酶及5-羟甲基胞嘧啶(5hmC)异常失衡这一关键表观遗传事件,系统梳理了其分子机制、功能影响及潜在干预策略。文章指出,胶质瘤尤其是胶质母细胞瘤中普遍存在5hmC整体下降和TET功能受损,TET1核排斥、TET2/TET3核内丰度下降与肿瘤恶性进展密切相关;同时,低TET2表达和低5hmC水平提示较差预后,而高TET3表达则与相对更好的临床结局相关。团队还总结了miRNA拮抗剂、维生素C、DNMT/HDAC抑制剂、CRISPR-dCas9表观编辑、脑穿透性IDH抑制剂等潜在治疗方向,并提出需进一步加强单细胞、空间组学和生物标志物研究。该成果为深入理解胶质瘤表观遗传异常及推进精准治疗提供了新的理论依据。

https://www.sciencedirect.com/science/article/pii/S1043661826000101?via%3Dihub
肖嵘团队揭示S-硫巯基化修饰调控系统性硬化症纤维化新机制
近日,中南大学湘雅二医院皮肤性病科肖嵘教授团队在美国风湿病学会官方期刊《关节炎与风湿病学》(Arthritis & Rheumatology)(IF 10.9)上发表题为《胱硫醚γ-裂解酶依赖的Smad3硫巯基化:系统性硬化症纤维化的新型治疗靶点》(《Cystathionine γ-lyase-dependent S-sulfhydration of Smad3: A novel target to alleviate fibrosis in systemic sclerosis》)的原创性研究成果,为系统性硬化症的靶向治疗提供新的理论依据和潜在干预策略。

研究团队首次发现,SSc患者中CSE/H₂S水平及整体S-硫巯基化水平显著降低,且CSE/H₂S表达水平与皮肤硬化程度呈负相关。功能实验证实,抑制或敲低CSE可显著促进成纤维细胞活化及细胞外基质沉积;而增强CSE表达或外源性补充H₂S则能有效抑制纤维化进程,并通过降低Smad3磷酸化水平、阻断其核转位及抑制下游转录活性等多个关键环节,显著抑制TGF-β1/Smad3信号通路的异常激活。体内实验进一步验证,通过腺相关病毒递送CSE基因可显著改善小鼠皮肤及肺部纤维化病变。上述结果表明,CSE/H₂S轴在SSc纤维化进程中发挥重要的内源性保护作用。
研究团队进一步通过S-硫巯基化修饰蛋白组学结合分子动力学模拟,首次鉴定Smad3为CSE介导S-硫巯基化的关键靶蛋白,并明确其Cys121位点是决定Smad3功能的重要分子开关。该修饰可改变Smad3与DNA结合的结构特性,调控其转录活性;而Cys121位点突变则显著削弱CSE的抗纤维化效应,揭示了S-硫巯基化在精细调控Smad3促纤维化功能中的关键作用。
王龙团队在高水平期刊《International Journal of Surgery》发表重要研究成果
近日,中南大学湘雅三医院泌尿外科王龙教授团队在国际外科学权威期刊《国际外科学杂志》(International Journal of Surgery,IF=10.1)发表题为《基于血浆代谢组学的良性前列腺增生关键代谢物发现与预测优化(Plasma Metabolomics Identifies Key Metabolites and Improves the Prediction of Benign Prostatic Hyperplasia)》的原创性研究论文。

良性前列腺增生(BPH)是影响中老年男性生活质量的常见病,随着全球人口老龄化的加剧,其早诊早治的需求愈发迫切。本研究打破了传统的局部视野,将BPH视为一种全身代谢性疾病进行深度解析。研究团队依托英国生物样本库(UK Biobank)近8万人的超大规模数据,并结合中国CHARLS队列进行跨人群验证,利用高通量核磁共振(NMR)代谢组学技术,对血浆中的143种代谢物进行了系统性深度扫描。通过融合先进的人工智能算法(XGBoost)与孟德尔随机化分析,团队不仅精准筛选出9种与BPH发病密切相关的核心代谢物,更从遗传学角度提供了因果证据。该研究提出的基于代谢组学的“生物学年龄”视角,刷新了对BPH复杂病因的认知,为实现高风险人群的早期识别与个体化精准干预提供了全新的生物学路标与技术支撑。
余正课题组在《Nature Microbiology》发表肠道微生物氨调控肠道神经与动力的原创性研究成果
近日,中南大学湘雅基础医学院人体微生物与健康课题组余正副教授团队在国际微生物领域顶级期刊《Nature Microbiology》(IF = 19.4)上在线发表题为 “Gut microbial ammonia enhances colonic acetylcholine levels to regulate intestinal motility” 的原创性研究成果。该研究系统揭示了肠道微生物来源的氨通过调控肠道神经递质乙酰胆碱(ACh)释放维持肠道蠕动和功能稳态的全新机制,为理解肠道微生物-神经-动力调控网络提供了重要理论突破。
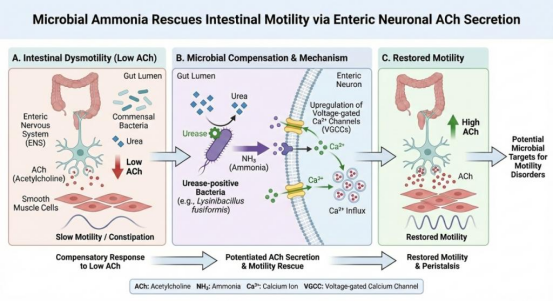
本研究发现,在乙酰胆碱缺乏和肠道动力受损状态下,肠道微生物会发生适应性代谢重塑,显著增强脲酶活性并提高氨的产生水平。研究团队通过动物模型和人群样本分析证实,微生物来源的氨能够显著提升结肠乙酰胆碱含量,改善肠道蠕动功能。机制研究进一步揭示,氨通过上调肠神经元突触前膜电压依赖性钙通道Cav2.1的表达,增强Ca²⁺ 内流,促进乙酰胆碱的释放,从而直接驱动肠道神经-肌肉传导。此外,研究团队从便秘患者粪便样本中分离获得一株具有强脲酶活性的菌株Lysinibacillus fusiformis,并证实其在体内可通过氨生成显著提升乙酰胆碱水平、恢复肠道动力。进一步构建的工程化脲酶表达菌株同样在动物模型中重现了上述效应,充分证明了“微生物-氨-肠神经递质”调控轴的因果关系和普适性。值得注意的是,本研究还系统评估了不同剂量氨干预的安全性,结果显示,生理相关浓度的氨可在不引起认知损伤的情况下显著改善肠道动力,揭示了氨在肠道局部环境中“信号分子”而非单纯“毒性代谢物”的双重属性。这一发现突破了传统认知,为重新理解肠道气体与微生物代谢在人体生理调控中的作用提供了新视角。
该研究首次提出肠道微生物可通过代谢补偿机制感知宿主神经递质变化,并以氨为信号分子维持肠道动力稳态,为便秘等肠道动力障碍的微生态干预提供了潜在新靶点,具有重要的基础研究价值和转化应用前景。
原文链接:https://www.nature.com/articles/s41564-026-02269-8
张永昌团队在发表“非小细胞肺癌免疫化疗给药时间的随机三期试验”的临床研究成果
近日,由湘雅医学院附属肿瘤医院张永昌教授团队作为第一通讯作者,该院作为第一完成单位在国际顶级医学期刊《Nature Medicine》(中科院一区TOP期刊,2024IF=50)在上发表了题为“Time-of-day immunochemotherapy in non-small cell lung cancer: a randomized phase 3 trial(非小细胞肺癌免疫化疗给药时间的随机三期试验)的原创性研究论文。
该研究聚焦于免疫治疗的“时辰效应”,通过一项前瞻性、随机对照、三期临床试验(LungTIME-C01),首次证实了给药时间可作为独立的、可调控的临床变量,对疗效产生关键影响。研究结果显示,对于晚期非小细胞肺癌患者,在下午3点之前给予免疫化疗,相比之后给药,可显著延长患者的无进展生存期与总生存期,疾病进展或死亡风险降低约60%,且不增加毒副作用。此项工作系统解决了“时辰治疗”在肿瘤免疫领域长期缺乏高水平前瞻性循证依据的关键问题,为提升现有免疫方案疗效,提供了一种简单、易行、无需增加治疗成本且具重要临床价值的优化路径,实现了“零花费,疗效倍增”的现实意义。

原文链接:http://dx.doi.org/10.1038/s41591-025-04181-w
倪千喜团队“一种混合AI策略在自动化放疗计划中的应用研究”的研究成果
近日,由湘雅医学院附属肿瘤医院倪千喜教授作为共同第一作者在自然子刊《Nature Communications》(中科院一区TOP期刊,2024IF=15.7)发表了题为“Multicenter study on the versatility and adoption of AI-driven automated radiotherapy planning across cancer types(人工智能驱动的自动化放疗计划在各类癌症中的通用性与应用多中心研究)”的原创性研究论文。
肿瘤放疗患者的放疗计划设计复杂且高度依赖医学物理师经验,导致计划质量和效率存在显著差异。尽管自动放疗计划技术(如协议优化、知识库计划等)已取得进展,但在实现临床可接受性、最优性和适用性三者平衡方面仍面临挑战。深度学习为自动计划(ATP)带来了新的机遇,但其如何最佳服务于临床实践,尤其是在多样化的临床环境中,尚需深入探索。
本研究成功开发并验证了一种高效、灵活的AI驱动自动放疗计划方案。多中心回顾性评估证实,该方案在多种癌症类型中不劣于人工计划,且能显著提升计划效率。研究强调了通过定制化临床目标列表适应不同临床环境的重要性,为ATP从单中心验证迈向多中心前瞻性临床应用提供了实用的方法论和坚实基础,有望推动放疗计划的标准化和普惠化。

原文链接:http://dx.doi.org/10.1038/s41467-025-67581-z
王静团队发表“呋喹替尼联合信迪利单抗治疗错配修复功能完整型晚期子宫内膜癌的多中心、单臂Ib/II期临床试验”的研究成果
近日,由复旦大学附属肿瘤医院吴小华教授、中南大学湘雅医学院附属肿瘤医院王静教授等领衔的多中心研究团队在国际知名学术期刊《Nature Communications》(中科院一区TOP期刊,2024IF=15.7)上发表了题为“Fruquintinib plus sintilimab in patients with advanced endometrial cancer with mismatch-repair proficient status: a multicenter, single-arm, phase Ib/II trial(呋喹替尼联合信迪利单抗治疗错配修复功能完整型晚期子宫内膜癌的多中心、单臂Ib/II期临床试验)”的重要研究成果。该研究首次系统评估了国产创新药呋喹替尼联合信迪利单抗在经治的错配修复功能完整(pMMR)型晚期子宫内膜癌患者中的疗效与安全性,填补了该领域在中国的治疗空白。
针对占子宫内膜癌群体约70%且缺乏有效二线治疗方案的pMMR型患者,该研究展现了显著的临床获益。数据显示,在98例经治晚期pMMR子宫内膜癌患者中,独立评审委员会(IRC)评估的客观缓解率(ORR)达到32.7%,疾病控制率(DCR)高达83.7%;中位无进展生存期(PFS)为8.6个月,中位总生存期(OS)达到21.8个月。这一疗效数据优于传统化疗或单药免疫治疗的历史数据(ORR约15%或更低),并与国际主流疗法(如仑伐替尼联合帕博利珠单抗)的疗效相当,且安全性可控,最常见3级及以上治疗相关不良事件为高血压(17.3%)。
该研究的创新性与价值在于:第一,确立了“抗血管生成+免疫治疗”双靶点联合策略在中国pMMR晚期子宫内膜癌患者中的有效性,为这一难治性人群提供了新的标准治疗选择;第二,基于此项关键注册临床研究结果,呋喹替尼联合信迪利单抗已在中国获得条件性批准,成为国内首个获批用于该适应症的抗血管生成药物联合PD-1抑制剂方案,解决了长期以来该类药物组合在国内未获批的临床急需;第三,研究证实无论患者PD-L1表达水平、既往是否接受过盆腔放疗或贝伐珠单抗治疗,均能从中获益,拓宽了受益人群范围。
这项由中国学者主导的高水平临床研究,不仅为晚期子宫内膜癌患者带来了新的生存希望,也标志着我国在妇科肿瘤创新药物研发与临床应用方面取得了重要突破,为全球子宫内膜癌治疗贡献了“中国方案”。

原文链接:http://dx.doi.org/10.1038/s41467-025-67375-3
于晓晖团队联合程岩团队发表“基于结构导向PROTAC策略靶向降解eEF2K治疗三阴性乳腺癌”的研究成果
近日,湘雅医学院附属肿瘤医院于晓晖团队联合湘雅二医院程岩教授团队在《Advanced Science》上发表题为“Targeted Degradation of eEF2K by a Structure‐Guided PROTAC Strategy for the Treatment of Triple-Negative Breast Cancer”(基于结构导向PROTAC策略靶向降解eEF2K治疗三阴性乳腺癌)的原创性研究论文。于晓晖教授为通讯作者,湘雅医学院附属肿瘤医院为第一单位。
蛋白水解靶向嵌合体(PROTAC)已成为一种有前景的抗癌药物类别。真核延伸因子2激酶(eEF2K)是一种应激反应型的翻译延长调节因子,已成为三阴性乳腺癌(TNBC)中的一个重要治疗靶点。本研究基于结构导向设计,针对eEF2K的非ATP结合口袋开发可有效降解eEF2K的PROTAC,其中降解效果最佳的化合物A6可通过构象优化的界面促进eEF2K降解,降解效率超90%。A6在TNBC细胞模型、裸鼠移植瘤以及TNBC类器官(PDO)模型中都展现出良好的抗肿瘤活性和可控的安全性。为进一步提升A6的降解效率并实现肿瘤靶向递送,研究团队以有机金属框架(MOF)类型的纳米粒构建了A6的PH敏感型纳米粒A6@ZIF-8。A6@ZIF-8表现出更佳的eEF2K降解效果,同时该纳米粒在肿瘤微环境酸性条件下可快速释放A6,从而显著提高肿瘤细胞内A6的积累,增强对eEF2K的降解作用和抗肿瘤效果。
该研究为TNBC提供了全新的精准治疗策略,将PROTAC靶向蛋白降解技术与智能纳米载体递送系统相结合,既有效改善了PROTAC理化性质不佳的问题,又提升了药物的肿瘤靶向性和生物利用度,为其他类型的PROTAC药物研发提供了重要参考。

原文链接:http://dx.doi.org/10.1002/advs.202520863
周慧俊团队发表“多功能荧光探针用于同时检测Cys、Hcy和超氧阴离子:揭示其在肿瘤氧化应激与铁死亡中的潜在应用”的研究成果
近日,由湘雅医学院附属肿瘤医院消化泌尿内一科周慧俊教授和湖南师范大学化学化工学院尹鹏教授作为共同通讯作者,在国际著名学术期刊《Science Advances》(中科院一区TOP期刊,2024IF=12.5)发表了题为“A fluorescent probe for concurrent detection of cysteine, homocysteine, and superoxide anion(多功能荧光探针用于同时检测Cys、Hcy和超氧阴离子:揭示其在肿瘤氧化应激与铁死亡中的潜在应用)”的原创性研究论文。
本研究深入探讨了半胱氨酸(Cys)、同型半胱氨酸(Hcy)和超氧阴离子(O₂•⁻)在肿瘤细胞氧化应激中的关键作用。氧化应激是推动肿瘤发生、进展及耐药性形成的关键因素,而Cys和Hcy的代谢重编程与肿瘤细胞的增殖及铁死亡抗性密切相关。O₂•⁻则在肿瘤的信号传导中发挥着复杂的双重作用。然而,现有技术难以同时、选择性地检测这三种分子,导致肿瘤相关的复杂调控网络长期未能完全揭示。
为填补这一空白,研究团队创新性地设计并合成了一种多功能荧光探针BPC,首次实现了对Cys、Hcy和O₂•⁻的高灵敏、多通道、实时可视化检测。该探针通过三个独立的荧光通道实现对目标分子的精准区分,成功应用于肿瘤细胞(如HeLa、HepG2、SH-SY5Y)、斑马鱼以及小鼠疾病模型中。此外,团队还开发了线粒体靶向版本BPC,能够在亚细胞水平上揭示肿瘤细胞在氧化应激状态下,线粒体内O₂•⁻和Hcy的异常升高以及Cys的耗竭。这一发现为解析肿瘤代谢重编程、铁死亡的调控机制以及肿瘤耐药性提供了全新的高时空分辨率工具。。
该研究不仅为揭示氧化应激与肿瘤细胞死亡之间的分子机制提供了创新的工具,而且为肿瘤的精准诊断、靶向治疗及新药筛选奠定了坚实的基础。这一突破性进展标志着肿瘤研究领域在分子成像技术上的一次重要飞跃,具有广阔的应用前景。
原文链接:http://dx.doi.org/10.1126/sciadv.adx6659




