近日,湘雅科研团队取得了多项突破。敲黑板!一起看看2026年3月的科研成果吧~
以下成果根据湘雅各二级学院、附属医院官网等整理。
陆前进、吴海竞团队联合清华大学教授团队在Nature发文揭示红斑狼疮免疫代谢发病新机制
李吉团队在《Cell》发表玫瑰痤疮原创研究成果
肖德胜、刘双和陶永光团队揭开微核真面目
董政、陈安群团队发文揭示DUSP26保护急性肾损伤新机制
蒋永芳、戴中上团队在权威期刊发文揭示酒精性肝硬化患者戒酒时机与社会经济因素的生存关联
王冰团队连续发表高水平研究成果
周宇团队在Journal of Advanced Research发表TBI相关肺损伤研究成果
周智广、赵斌、黄佳琦团队在《Molecular Therapy》发表1型糖尿病免疫调控研究重要进展
王先成团队系统阐述多尺度血管工程相关进展
冯也倩团队系统阐述重塑肿瘤细胞因子网络增强免疫检查点阻断新策略
谢小燕团队研发了一款智能响应型壳核微针药物递送系统用于治疗慢性牙周炎
梁青春团队通过整合肿瘤微环境特征的深度学习框架准确预测肺癌病理图像中的多个驱动基因突变
胡招兰团队发表高水平综述系统阐述类风湿关节炎精准诊疗分析策略
马晓伟团队联合发表了阿尔茨海默病最新研究成果
湘雅二医院耳鼻咽喉头颈外科团队在《Materials Today Bio》发表头颈部鳞癌铁死亡靶向治疗研究成果
湘雅口腔医学团队在国际期刊《Materials Today Bio》发表综述阐述粘附性水凝胶口腔治疗应用前景
罗静团队在《Diabetologia》发表糖尿病视网膜病变新成果
陈世杰、李劲松团队在《Bioactive Materials》发表研究成果
余正团队发表肠道微生物氨调控肠动力的原创成果
周文虎、刘俊彦团队在《Acta Pharmaceutica Sinica B》发表骨关节炎靶向治疗最新研究成果
李发祥课题组研究揭示细菌抗噬菌体防御的分子机制
陆前进、吴海竞团队联合清华大学教授团队在Nature发文揭示红斑狼疮免疫代谢发病新机制
近日,中国医学科学院皮肤病医院、中南大学湘雅二医院特聘教授陆前进教授及中南大学湘雅二医院、芙蓉实验室吴海竞教授,联合清华大学生命学院、清华-北大生命科学联合中心刘万里教授、清华大学药学院张永辉教授等团队,在国际学术期刊《自然》(Nature,IF=48.5,Q1)发表题为“角质形成细胞的代谢警报素增强系统性体液免疫”(A metabolic alarmin from keratinocytes potentiates systemic humoral immunity)的原创性研究论文;同时在《免疫与炎症》(Immunity & Inflammation)发表题为“芳香型TRPV3激动剂作为可滴定的有机佐剂增强抗原特异性IgG应答”(Fragrant TRPV3 agonists act as titratable organic adjuvants to amplify antigen-specific IgG response)的相关研究论文。
此攻关团队揭示角质形成细胞(KC细胞)来源的甲羟戊酸通路代谢中间物(法尼基焦磷酸FPP)作为内源性警报素,从病灶局部快速高效的通过TRPV3,激活Ca2+-CaM-Calcineurin-NFAT和PYK2–RAS–ERK通路,调控系统体液免疫应答的新型机制;团队还揭示香芹酚、樟脑酮等药用植物来源的外源性芳香类的TRPV3激动剂,也通过TRPV3-Ca2+信号轴放大抗原特异性抗体应答;这样“一内一外”的内源性代谢警报素与外源性感觉芳香素相辅相成的双模TRPV3激活信号转导体,为新型疫苗佐剂的研发和系统性红斑狼疮(SLE)等自身免疫病的防治提供潜在靶点和思路。

李吉团队在《Cell》发表玫瑰痤疮原创研究成果
近日,中南大学湘雅医院李吉教授、邓智利教授团队联合山东大学孙金鹏教授、郭璐璐教授团队合作,在玫瑰痤疮的代谢调控机制与靶向药物开发方面取得重要突破。该研究实现了从“临床代谢组学—疾病发生机制—受体信号转导机制—人工智能辅助药物设计”的完整研究路径,首次揭示了靶向代谢通路干预玫瑰痤疮血管功能障碍的分子机制,并基于酮戊二酸受体1(OXGR1)这一新靶点开发了新型激动剂,为解决玫瑰痤疮持续性红斑这一临床难题提供了全新的精准治疗策略。相关成果以“代谢物调控的血管收缩‘开关’:OXGR1激活机制推动玫瑰痤疮红斑靶向激动剂的治疗策略”为题,于3月5日在《Cell》(细胞)杂志发表。

玫瑰痤疮是一种多发于面部的慢性炎症性皮肤病,极易反复发作,严重影响患者身心健康,全球患病率约5.5%。玫瑰痤疮最突出的临床特征是顽固性持续性红斑,目前针对该红斑的治疗手段有限、疗效不佳且副作用显著,是亟待解决的核心临床痛点,亟须探索安全、高效的新型治疗策略。血管异常扩张是产生持续性红斑的主要病理机制,研究表明,血管稳态易受到循环代谢状态的影响,团队前期的研究也证实玫瑰痤疮患者存在系统性的代谢紊乱。因此,团队将研究方向聚焦于玫瑰痤疮的代谢调控机制。
研究团队基于临床代谢组学分析,发现玫瑰痤疮患者血清中关键代谢物α-酮戊二酸(α-KG)升高,且与红斑严重程度呈正相关。机制研究表明,α-KG通过特异性结合并激活血管平滑肌细胞膜上的G蛋白偶联受体(GPCR)OXGR1,进而激活Gq信号通路,增强肌球蛋白轻链激酶(MLCK)依赖的肌球蛋白轻链9(MYL9)磷酸化。该信号级联反应可促进血管平滑肌收缩,有效抑制病理性血管扩张,从而缓解小鼠的玫瑰痤疮样红斑表型。这提示α-KG的升高可能是一种代偿性保护反应,而外源补充α-KG可进一步增强该保护效应。
为进一步阐明OXGR1的活化机制,研究团队探究了OXGR1识别α-KG/衣康酸(ITA)以及受体激活的分子机制。分析揭示了OXGR1区别于经典GPCR的独特双酸识别口袋及配体识别模式。基于该结构基础,研究团队应用人工智能辅助的方法设计并合成了一种兼具高活性与高选择性的新型OXGR1特异性激动剂A-1。体内实验证实,低剂量A-1即可显著改善小鼠红斑表型,疗效与临床一线药物溴莫尼定相当,且具备更高的安全性。
肖德胜、刘双和陶永光团队揭开微核真面目
近日,中南大学湘雅医院病理科肖德胜教授、刘双教授和陶永光研究员团队在细胞信号转导与靶向治疗领域国际顶级期刊《Signal Transduction and Targeted Therapy》(信号转导与靶向治疗,IF=52.7)发表题为《Micronuclei: origins, assays, mechanisms, diseases and treatments》(微核:起源,检测,机制,疾病与治疗)的重磅综述文章。该研究系统全面梳理微核研究进展,深入阐释其起源、检测方法、形成机制,以及在肿瘤等多种疾病发生发展中的作用和潜在治疗应用,为相关疾病精准诊疗提供重要理论依据与全新研究方向。

在细胞内部,除了承载主要遗传物质的主细胞核,有时还会出现一些微小的、独立的核样结构,它们被称为“微核”。长期以来,微核被视为细胞DNA损伤或分裂异常的“伤痕”与“标志物”。然而,近几年的研究指出,微核已不再仅仅是基因组不稳定的结果,其本身已成为主动加剧染色体不稳定性、驱动疾病进展(尤其是癌症)的关键推手。这一认知的转变为理解肿瘤发生、发展及探索新型治疗策略提供了全新视角。
此次发表的综述回溯微核研究百年历史,详细阐述其三大核心形成机制——有丝分裂缺陷导致的染色体滞后、DNA双链断裂、核出芽,同时系统解析微核形成后的五大命运走向:重新整合入主核、细胞质中持续存在、膜破裂、降解及外排,并深入阐明各命运背后的分子调控通路与关键作用因子。
董政、陈安群团队发文揭示DUSP26保护急性肾损伤新机制
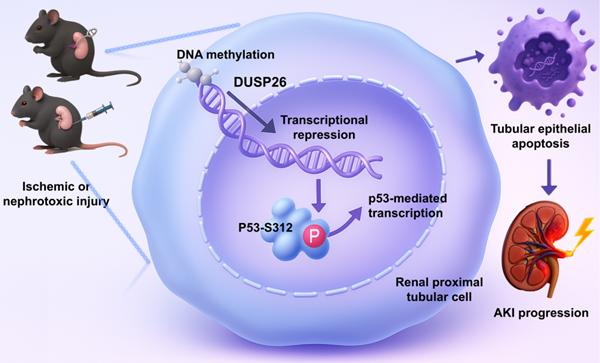
近日,中南大学湘雅二医院特聘教授董政与陈安群教授团队在国际学术期刊《自然·通讯》(Nature Communications,IF 15.7)发表题为《DUSP26通过去磷酸化p53 Ser312位点减轻急性肾损伤》(DUSP26 protects against acute kidney injury by dephosphorylating p53 at serine 312)的原创性研究论文。该研究系统揭示了双特异性磷酸酶DUSP26通过去磷酸化p53 Ser312抑制肾小管细胞损伤与凋亡、从而减轻急性肾损伤的新机制,为急性肾损伤的精准干预提供了新的理论基础和潜在靶点。
研究发现,DUSP26在AKI患者肾组织以及顺铂诱导、缺血再灌注诱导的小鼠AKI模型中均显著下调。进一步机制研究表明,这一下调与DUSP26启动子高甲基化密切相关。在损伤状态下,DNMT1和DNMT3A被招募至DUSP26启动子区域,促进其甲基化并导致转录沉默,进而削弱DUSP26对肾小管细胞的保护作用。在功能层面,研究团队通过体内外多种模型证实,DUSP26具有明确的肾脏保护作用。DUSP26缺失可显著加重肾小管损伤,而在近端肾小管中特异性恢复DUSP26表达,则可明显改善肾功能并减轻组织损伤。进一步研究显示,DUSP26的保护效应严格依赖其磷酸酶活性,当其活性位点突变后,这一保护作用明显减弱。
更为重要的是,研究团队从机制上阐明了DUSP26-p53这一关键调控轴。研究证实,DUSP26可直接结合p53,并特异性去磷酸化其Ser312位点,从而抑制p53对细胞死亡相关基因的转录激活,减轻肾小管上皮细胞凋亡与损伤。相反,当DUSP26下调时,p53 Ser312位点磷酸化增强,促凋亡转录程序被激活,最终推动AKI进展。该研究由此建立了“DUSP26下调—p53异常激活—肾小管损伤加重”的关键机制线索。
蒋永芳、戴中上团队在权威期刊发文揭示酒精性肝硬化患者戒酒时机与社会经济因素的生存关联
近日,中南大学湘雅二医院蒋永芳教授、戴中上主治医师团队在肝脏病学领域顶刊《肝脏学杂志》(Journal of Hepatology, IF 33)发表重要研究成果“早期戒酒、社会经济障碍与失代偿期酒精性肝硬化患者的生存预后:一项来自中国的真实世界队列研究”(Early Abstinence, Socioeconomic Barriers, and Survival in Decompensated Alcohol-Related Cirrhosis: A Real-World Cohort from China),首次基于中国真实世界队列,系统探究酒精性肝硬化患者早期戒酒、社会经济壁垒与生存预后的关联,为该疾病在中低收入地区的临床管理和公共卫生干预提供了关键的本土化证据。
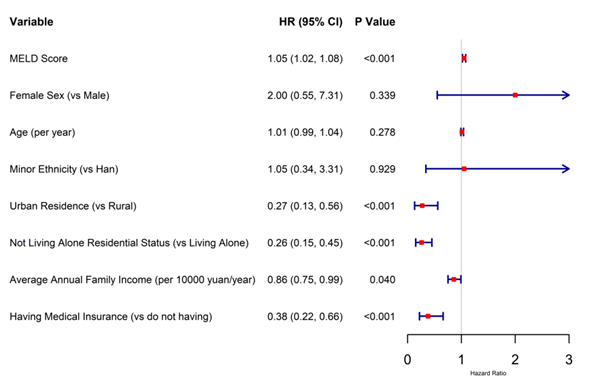
本研究的核心发现具有重要的临床和公共卫生意义。一方面,团队证实早期戒酒是中国酒精相关肝硬化患者生存获益的强预测因子,为亚洲人群该疾病的临床管理策略提供了关键的外部验证证据;另一方面,研究首次探讨酒精相关肝硬化的预后不仅取决于肝损伤的生物学严重程度和戒酒行为本身,还深受患者社会支持网络和经济资源获取能力的影响。本研究提示,临床实践中亟需开展整合式多学科干预,同时解决患者戒酒面临的医疗和社会层面障碍,此举将为改善中低收入地区酒精相关肝硬化患者的预后提供重要助力。
王冰团队连续发表高水平研究成果
近日,中南大学湘雅二医院脊柱外科、湖南省数字化脊柱外科临床中心王冰教授领衔团队连续发表多篇高水平文章,围绕脊髓损伤、椎间盘退变再生、临界尺寸骨缺损修复及老年健康工程等前沿科学问题,系统揭示了多种组织再生与微环境调控新机制,为脊柱退行性疾病的精准干预提供了新的理论基础与临床转化策略。
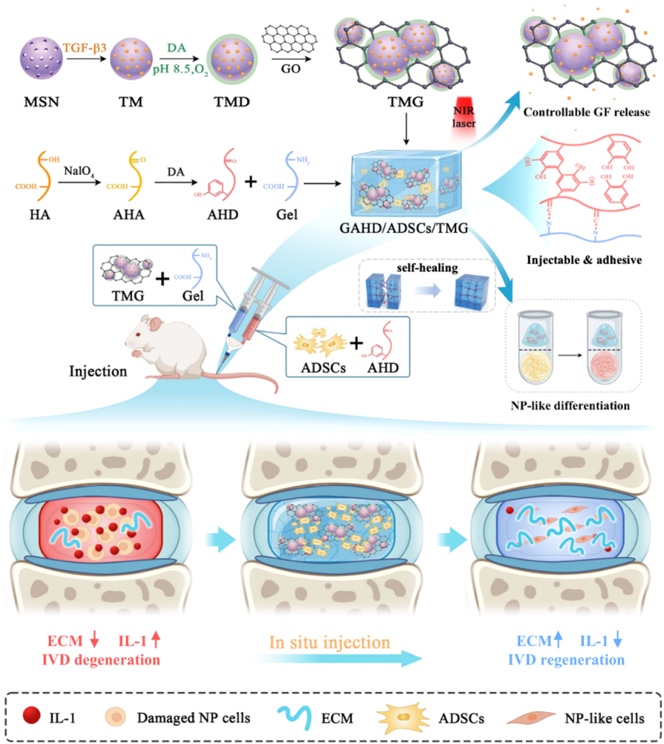
在Chemical Engineering Journal《化学工程杂志》(中科院一区Top期刊,IF=13.2)发表题为“Injectable self-healing hydrogel for co-delivery of stem cells and growth factors in intervertebral disc regeneration”(用于椎间盘再生中干细胞和生长因子共递送的可注射自修复水凝胶)的原创性研究论文,涂志明主治医师、袁涛助理研究员及孙维楚博士为论文共同第一作者,王冰教授、李亚伟副主任医师等为共同通讯作者,中南大学为第一作者及通讯作者单位。该研究构建明胶-多巴胺氧化透明质酸自愈合水凝胶,负载GO包被MSN实现TGF-β3近红外控释,为椎间盘退变提供了微创、可控释放的精准再生策略。
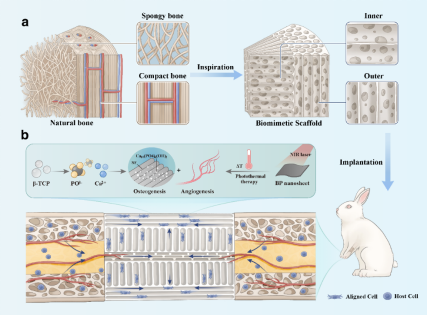
在Journal of Nanobiotechnology《纳米生物技术杂志》(中科院一区Top期刊,IF=14.78)期刊上发表了题为“Hierarchical biomimetic scaffold with directional guidance and photothermal properties for the repair of critical-sized bone defects”(兼具引导及光热特性的层级仿生支架在临界性骨缺损修复中的应用)的原创性研究论文,博士研究生罗李、助理研究员袁涛为论文共同第一作者,王冰教授与浙江省农科院杨磊教授、国科温州研究院汪雨教授为该文共同通讯作者,中南大学为第一作者及通讯作者单位。该研究利用改进定向冷冻铸造技术构建分级仿生支架,协同β-TCP纳米颗粒与黑磷纳米片,为先进骨再生生物材料的设计提供了有效且创新的设计范式。
周宇团队在Journal of Advanced Research发表TBI相关肺损伤研究成果
近日,神经外科周宇团队在《Journal of Advanced Research》(TOP双一区期刊,IF=13)发表研究论文《Mesenchymal stem cell transplantation alleviated TBI-induced lung injury by inhibiting PAD4-dependent NET formation》,揭示了人脐带来源间充质干细胞(hUC-MSCs)缓解创伤性脑损伤(TBI)继发肺损伤的新机制。

研究发现,TBI患者外周血及支气管肺泡灌洗液中中性粒细胞明显活化,NETs形成增加,且肺部中性粒细胞浸润程度与肺损伤严重程度显著相关。在小鼠TBI模型中,hUC-MSCs治疗可改善神经功能,减轻脑及肺组织损伤,提高血氧饱和度,并抑制中性粒细胞浸润、NETs形成及PAD4表达。体外实验进一步证实,hUC-MSCs可直接抑制TBI患者中性粒细胞NETs生成和活性氧释放。该研究为揭示TBI相关肺损伤的发病机制提供了新证据,也为间充质干细胞在TBI继发肺部并发症中的临床转化应用提供了新的理论依据。
周智广、赵斌、黄佳琦团队在《Molecular Therapy》发表1型糖尿病免疫调控研究重要进展
近日,中南大学湘雅二医院国家代谢性疾病临床医学研究中心周智广教授、赵斌教授、黄佳琦教授团队在国际基因与细胞治疗权威期刊《分子治疗》(Molecular Therapy,IF=12.4)发表题为《固有免疫细胞来源的BAFF通过激活非经典NF-κB通路促进糖尿病自身免疫中ICOSL+ B细胞的炎症反应》(Innate immune cell-derived BAFF induces non-canonical NF-κB activation to promote inflammatory response of ICOSL+ B cells in diabetic autoimmunity)的原创性研究论文。

1型糖尿病(T1D)是一种因免疫耐受紊乱导致胰岛β细胞受损的自身免疫性疾病,虽已知B细胞在其中扮演关键角色,但现有靶向疗法仍面临精准度不足的瓶颈。本研究打破了对B细胞功能的常规认知,聚焦于免疫检查点分子ICOSL,深度解析了ICOSL⁺B细胞在T1D病程中的“免疫桥梁”作用。研究团队依托多维度临床队列(涵盖健康供体、经典T1D、LADA及T2D患者)并结合NOD小鼠模型,利用转录组测序、多参数流式细胞术及功能学实验,对ICOSL⁺B细胞的表型演变与调控机制进行了全方位系统解析。
研究发现,ICOSL⁺B细胞在T1D患者外周血中显著升高,且能精准预警β细胞功能的快速衰退。通过融合RNA测序与分子生物学手段,团队首次揭示了由固有免疫细胞分泌的BAFF通过激活非经典NF-κB信号轴,驱动ICOSL⁺B细胞恶性扩增与促炎转化的分子逻辑。更具临床意义的是,研究证实联合靶向ICOSL与BAFF可产生显著的协同治疗效应,有效延缓糖尿病进展并减轻胰岛炎症。该研究提出的“固有免疫-BAFF-ICOSL⁺B细胞-T细胞”轴线理论,刷新了对糖尿病免疫发病机制的系统性认知,为实现T1D的早期预后评估与个体化精准免疫干预提供了全新的生物学路标与战略靶点。
王先成团队系统阐述多尺度血管工程相关进展
近日,中南大学湘雅二医院王先成教授团队在国际知名期刊《Chemical Engineering Journal》(IF:13.2)发表题为“Advancing multiscale vascular engineering for regeneration and transplantation”的综述文章。该研究系统梳理了血管工程领域从宏观组织工程到微尺度类器官的技术演进,提出多尺度整合的新研究范式。

血管系统作为组织再生的核心基础,其层级结构从大血管延伸至毛细血管网络,对组织存活与功能恢复具有决定性作用。该综述从血管组织工程、组织工程血管化、血管类器官及类器官血管化四个层面,系统总结了近年来细胞工程、生物材料及生物制造技术的关键进展。文章指出,传统血管工程主要聚焦结构替代,而当前研究正逐步转向“结构—功能一体化重建”。其中,iPSC来源细胞、多组分水凝胶及3D生物打印、微流控等技术的融合,为构建具有灌注能力和生理响应特性的血管网络提供了重要支撑。
此外,作者强调血管类器官作为“微循环模块”的重要价值,其自组织能力与体内整合潜力,使其成为连接不同尺度血管构建策略的关键桥梁。该综述从跨尺度角度建立了统一的血管工程理论框架,为再生医学和器官构建提供了新的研究方向。
原文链接https://doi.org/10.1016/j.cej.2026.175126
冯也倩团队系统阐述重塑肿瘤细胞因子网络增强免疫检查点阻断新策略
近日,中南大学湘雅二医院肿瘤科冯也倩教授团队在国际期刊《Journal of Experimental & Clinical Cancer Research》(IF:12.8)发表题为“Rewiring tumor cytokine networks to enhance immune checkpoint blockade: mechanisms, engineering, and clinical translation”的综述论文。该文系统总结了肿瘤微环境中细胞因子网络与免疫检查点阻断治疗之间的复杂互作关系,全面梳理了通过重塑细胞因子网络提升肿瘤免疫治疗疗效的研究进展,为克服免疫治疗耐药、拓展优势人群提供了新的理论依据与转化思路。
免疫检查点抑制剂近年来在多种实体瘤治疗中取得显著进展,但临床实践中仍有相当一部分患者存在原发或继发耐药,限制了其长期获益。肿瘤微环境中的细胞因子网络是影响抗肿瘤免疫应答的重要调控枢纽,既可通过促进T细胞活化、增殖和杀伤增强抗肿瘤效应,也可能通过诱导免疫抑制、促进炎症逃逸和肿瘤进展削弱治疗效果。因此,如何精准调控细胞因子网络、逆转免疫抑制性肿瘤微环境,已成为提高免疫检查点阻断疗效的重要研究方向。
该综述围绕“细胞因子网络重塑联合免疫检查点阻断”这一主题,系统归纳了促炎性细胞因子和免疫抑制性细胞因子在肿瘤免疫中的双重作用。一方面,IL-2、IL-12、IL-15及I型/II型干扰素等促炎性细胞因子可增强CD8+T细胞和自然杀伤细胞功能,促进肿瘤免疫激活;另一方面,IL-6、TGF-β、IL-1β及IL-10等免疫抑制性因子则可驱动免疫逃逸、T细胞功能耗竭及肿瘤微环境重塑,成为免疫治疗抵抗的重要机制。论文进一步指出,通过靶向抑制免疫抑制性细胞因子通路、优化促炎性细胞因子递送方式,有望将“冷肿瘤”转化为“热肿瘤”,从而提升免疫检查点抑制剂的治疗敏感性。
在治疗策略方面,文章重点总结了近年来该领域的重要研究进展,包括天然细胞因子及工程化细胞因子激动剂、免疫细胞因子融合蛋白、受体选择性设计、局部给药平台、病毒与基因治疗载体,以及针对IL-6、TGF-β、IL-1β、CXCR4和VEGF等抑制性通路的联合治疗方案。综述认为,未来应更加重视生物标志物指导下的患者筛选、毒性管理及系统层面的动态建模,以识别更具临床价值的干预节点,推动细胞因子调控与免疫检查点阻断治疗的精准联合。
该论文的发表,体现了湘雅二医院肿瘤科在肿瘤免疫治疗与转化研究领域的持续积累。相关成果不仅有助于深化对肿瘤免疫微环境调控机制的认识,也为肿瘤免疫联合治疗策略的优化提供了重要参考,具有积极的学术意义和潜在临床应用价值。
谢小燕团队研发了一款智能响应型壳核微针药物递送系统用于治疗慢性牙周炎
近日,中南大学湘雅二医院口腔医学中心谢小燕博士团队在国际知名期刊《纳米生物技术杂志》(Journal of Nanobiotechnology)(IF 12.6)上发表题为《用于牙周炎骨修复的具有MMP/pH触发释放功能的核壳微针》(《Core–shell microneedles with MMP/pH-triggered release for periodontitis bone repair》)的原创性研究成果,为应对牙周炎治疗的挑战提供了一种极具前景的新策略。

牙周炎是由牙周致病菌引发的局部炎症,其特征是牙槽骨不均匀吸收。牙周炎微环境的特征包括致病菌过度生长、巨噬细胞极化平衡紊乱、炎症介质过度分泌、基质金属蛋白酶(MMP)活性失调以及局部pH值失调等。持续的炎症环境与骨再生需求之间的冲突使牙周炎的治疗变得复杂。为了解决这一问题,谢小燕博士团队研发了一款核壳型微针药物递送系统,该系统能够响应牙周病变的病理特征——高表达的基质金属蛋白酶(MMP)和局部酸性微环境。该系统利用MMP水解和pH触发的双重机制,实现治疗分子的精确时空释放和多模式协同治疗。该微针系统采用分层核壳结构:外壳负载甘草酸功能化的MIL-101,包裹着含有间充质干细胞来源外泌体的核心层。在治疗初期,当MMP水平升高且pH值降低时,该系统可迅速从微针外壳释放载药纳米颗粒,从而显著抑制促炎细胞因子风暴并减轻过度氧化应激。随后,从微针芯持续释放的外泌体有助于重新平衡免疫微环境,并在牙周缺损处诱导新骨形成。这种新型药物递送策略通过整合病理微环境响应性,将精准药物递送、免疫调节和牙周炎相关骨缺损的组织再生相结合,从而克服了在复杂口腔环境中实现药物梯度释放的挑战,并为临床治疗提供了一种创新的治疗模式。
梁青春团队通过整合肿瘤微环境特征的深度学习框架准确预测肺癌病理图像中的多个驱动基因突变
中南大学湘雅二医院梁青春及湖南大学彭绍亮共同通讯在Cancer Research(IF=12.5)在线发表题为“A Deep Learning Framework Integrating Tumor Microenvironmental Features Accurately Predicts Multiple Driver Gene Mutations in Lung Cancer Pathology Images”的研究论文。该研究收集了来自中国四家医院2573例肺癌患者的配对病理图像与二代测序数据,构建了一个大型多中心数据集。基于此,作者开发了NAVF-Bio——一种基于多示例学习的自适应多视角特征融合框架,能够整合全切片图像(WSI)中的肿瘤微环境(TME)特征,以预测驱动突变及肿瘤突变负荷(TMB)。
通过对11种前沿深度学习方法的基准测试,NAVF-Bio在预测驱动突变(TP53、EGFR、KRAS、ALK)和TMB状态方面均持续优于现有模型,并在外部多中心验证中达到临床相关性能。值得注意的是,NAVF-Bio能够跨中心准确预测突变驱动基因的外显子区域,同时基于WSI可视化与TME定量分析的可解释性研究进一步证实了该框架解析病理相关肿瘤特征的能力。最后,作者构建了面向肺癌的多基因突变预测平台,以促进驱动基因突变的筛查。总体而言,NAVF-Bio通过观察WSI的多尺度特征与TME特性来预测肺癌驱动基因突变,模拟了病理学家阅片的工作流程,有望为患者靶向治疗的选择提供指导。
原文链接:https://doi.org/10.1158/0008-5472.CAN-25-0582
胡招兰团队发表高水平综述系统阐述类风湿关节炎精准诊疗分析策略
近日,中南大学湘雅二医院胡招兰教授团队受主编特邀,在国际知名学术期刊《Trends in Analytical Chemistry》(JCR Q1,影响因子:12.0)上发表了题为“Analytical strategies for rheumatoid arthritis diagnosis and monoclonal antibody‑based therapy: From biomarkers to therapeutic drug monitoring”(类风湿关节炎诊断与单抗治疗的分析化学策略:从生物标志物到治疗药物监测)的重要综述论文。该研究系统解析了类风湿关节炎(RA)在血清学诊断、单抗药物治疗监测及标准化分析中面临的核心挑战与前沿技术进展。
1. RA诊疗“分析瓶颈”,揭示多平台协同新路径:RA生物标志物(如类风湿因子、抗环瓜氨酸肽抗体)存在低丰度、高异质性及抗体多样性等难题,传统免疫分析方法灵敏度与特异性受限。同时,单抗类药物(如抗TNF-α、IL-6抗体)因患者个体差异、免疫原性及抗药抗体干扰,导致疗效不一。该团队详细绘制了涵盖三大分析平台的“技术全景图”:
①先进免疫分析:包括时间分辨荧光能量转移(TR-FRET)、多重ELISA等,实现高通量、高信噪比的多指标同步定量。
②生物传感器与适体检测:基于表面等离子体共振(SPR)、生物层干涉(BLI)及电化学适体传感器,实现无标记、实时动力学监测;CRISPR-Cas系统的引入进一步将检测限推进至摩尔级别。
③分子成像探针:靶向活性氧(ROS)和次氯酸(HClO)的探针可原位可视化关节局部炎症,弥补系统性血清标志物的空间信息缺失。
2. 精准用药“新哨兵”:针对单抗治疗中药物浓度变异大、抗药抗体干扰严重的问题,团队系统评估了LC-MS/MS与免疫分析的互补优势。LC-MS/MS通过特征肽段检测实现高特异性、多药联检,而免疫分析快速灵敏但易受基质干扰。提出采用酸解离-桥联免疫法或质谱表位作图策略,提升抗药抗体检测的准确性与耐药区分能力。同时强调严格基质校正、标准化参考物质及跨平台校准是实现治疗药物监测临床转化的前提。基于此,团队自主研发的神经营养因子类抗体药目前和药企正在并进行上下游工艺放大确认、分析方法验证,预期在未来3-5年内逐步完成全部临床前研究及中试生产。
3. 未来方向:AI赋能多模态融合检测
综述进一步展望了精准风湿病学的三大前沿趋势:多模态数据整合(空间单细胞分析、组学谱与成像)、床旁即时检测设备(微流控SPR、可穿戴微针适体传感器)以及多模态联合诊断(联合治疗药物监测、抗药抗体谱及人工智能辅助决策)。作者指出,先进分析平台与临床实践的深度融合,将为RA患者实现真正个体化的长期治疗管理提供有力支撑。
该综述为RA早期诊断、疗效监测及抗药抗体评估提供了系统的分析化学解决方案,对推动精准风湿诊疗标准化具有重要参考价值。
原文链接:https://www.sciencedirect.com/science/article/pii/S0165993626001585
马晓伟团队联合发表了阿尔茨海默病最新研究成果
近日,中南大学湘雅二医院核医学科马晓伟团队联合复旦大学附属华山医院核医学/PET中心管一晖/谢芳团队、上海交通大学医学院附属第六人民医院转化医学中心贾伟/陈天璐团队,老年科郭起浩团队在《Alzheimer’s & Dementia》(影响因子11.1)发表了题为《胆汁酸与阿尔茨海默病患者基线和纵向淀粉样蛋白和tau病理存在关联》(Bile acids are associated with baseline and longitudinal amyloid and tau pathology in patients with Alzheimer’s disease)的研究性论文。从病理层面拓展了胆汁酸在AD发生发展中的作用,不仅再次印证了“肠道菌群-胆汁酸-脑轴”理论,更具体勾勒出了DCA和LCA家族参与Aβ和Tau蛋白沉积的病理蓝图。为AD的血液学诊断和预测提供了全新的高优候选标志物,也为未来开发靶向“肠-脑轴”的AD治疗药物指明了攻坚方向。
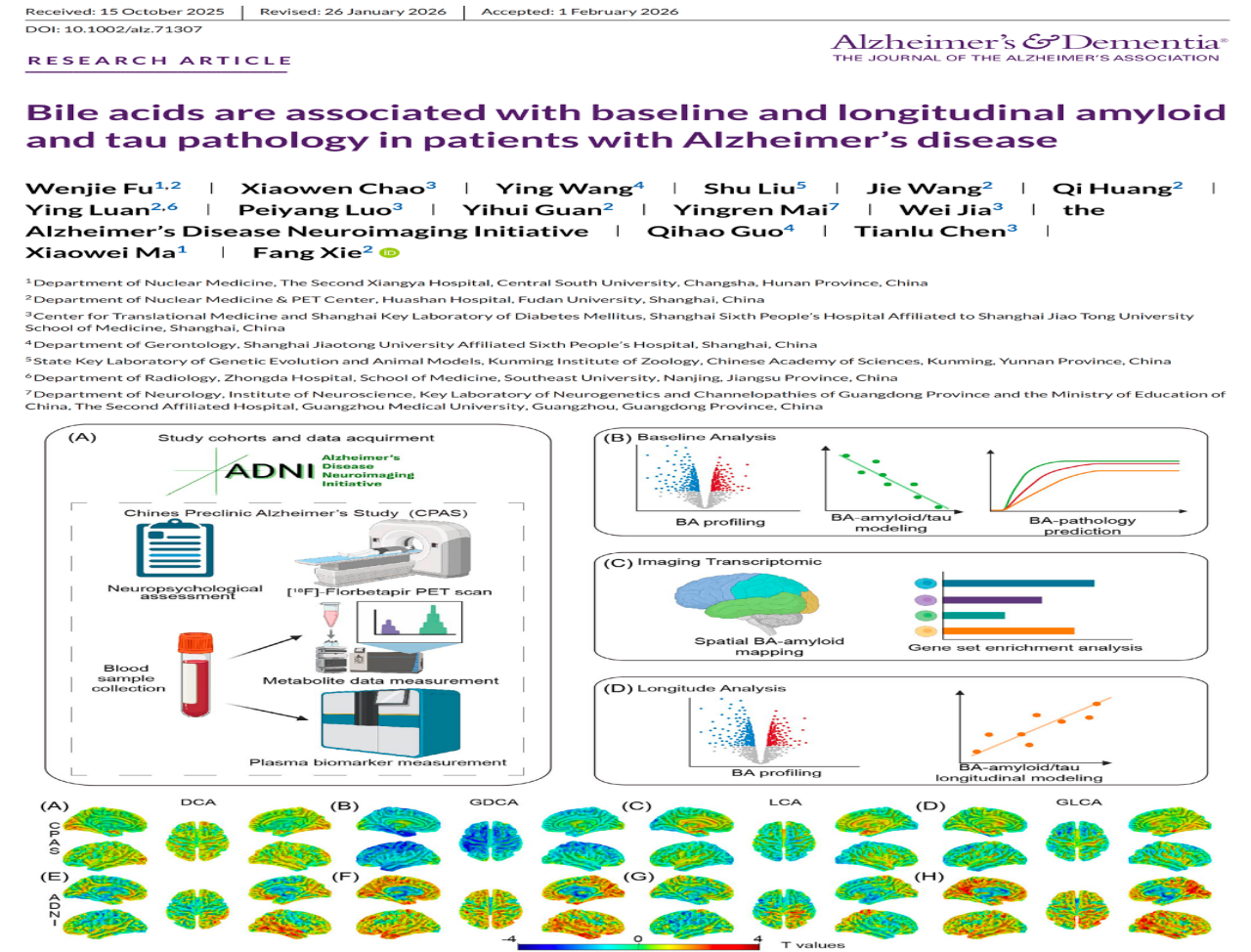
阿尔茨海默病(AD)是一种复杂的神经退行性疾病,其核心病理特征是细胞外淀粉样蛋白(Aβ)的聚集与细胞内Tau蛋白的过度磷酸化,但这些大脑深处的病理改变并非孤立发生。近年来,代谢功能障碍,尤其是肠脑轴在AD发病机制中的作用正受到极大的关注。
近日,以上团队聚焦于AD病理分期和进展,对中国CPAS和美国ADNI两个超千人队列的胆汁酸谱进行了系统研究。发现脱氧胆酸(DCA)和石胆酸(LCA)两个次级胆汁酸家族与基线病理指标、两年内病理指标的进展密切相关。从影像转录组层面解释了它们经由(1)线粒体功能与能量代谢:涉及神经冲动传导、质子跨膜运输以及线粒体呼吸链复合体Ⅰ的组装;(2)神经活性配体受体信号传导及免疫调节:包括MAPK信号通路和钙信号通路参与调节Aβ沉积的作用机制。这些证据表明,胆汁酸并非通过单一途径起效,而是通过诱发线粒体功能障碍、能量代谢异常以及调节神经炎症和突触功能等多重机制,驱动了AD病理的进展。这一研究为AD的血液学诊断和预测提供了一个全新的高优候选标志物—胆汁酸,为未来开发靶向“肠-脑轴”的AD治疗药物提供了一个新的方向。
湘雅二医院耳鼻咽喉头颈外科团队在《Materials Today Bio》发表头颈部鳞癌铁死亡靶向治疗研究成果
近日,中南大学湘雅二医院耳鼻咽喉头颈外科中心耳鼻咽喉头颈肿瘤研究室团队在生物材料领域期刊《Materials Today Bio》(IF=10.2)发表了题为“An exosome-biomimetic photothermal nanocarrier for IGF2BP2 siRNA delivery and enhanced ferroptosis in head and neck squamous cell carcinoma”的研究论文。论文第一作者及通讯作者单位均为中南大学湘雅二医院,团队李仕晟副教授为通讯作者,李蒙蒙博士为第一作者。
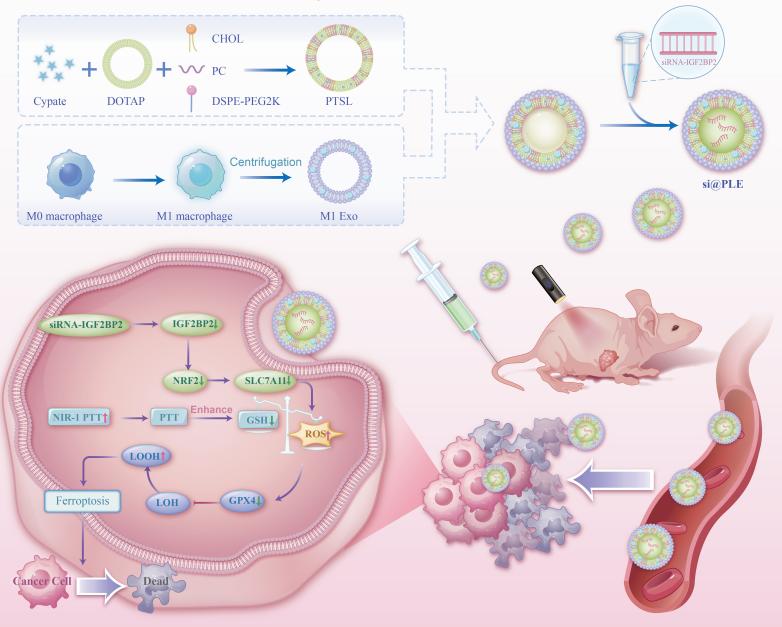
头颈部鳞癌治疗耐药是临床核心难题,铁死亡是极具潜力的新型治疗方向,但调控机制与递送技术长期存在瓶颈。本文揭示,RNA结合蛋白IGF2BP2通过调控NRF2抗氧化轴,介导头颈部鳞癌铁死亡耐药,明确了新的治疗靶点。基于这一发现,团队创新性构建外泌体仿生光热纳米载体(si@PLE),融合M1巨噬细胞外泌体与光热响应脂质体,靶向递送IGF2BP2 siRNA,实现基因沉默与光热治疗的协同增效。体内外实验证实,该载体可显著增强肿瘤铁死亡、抑制肿瘤生长,且安全性良好。该研究成功建立了“仿生基因沉默-光热治疗”协同平台,为克服头颈部鳞癌治疗耐药、实现精准靶向治疗提供了重要的理论依据与转化前景。
湘雅口腔医学团队在国际期刊《Materials Today Bio》发表综述阐述粘附性水凝胶口腔治疗应用前景
近日,中南大学湘雅二医院口腔医学中心谢小燕博士,联合长沙市口腔医院、浙江树人大学等科研团队,在国际权威学术期刊《Materials Today Bio》(影响因子10.2)上,在线发表了题为《Designing adhesive hydrogels for oral diseases treatment》(设计用于口腔疾病治疗的粘附性水凝胶)的学术论文。该研究从分子、网络、系统三个层面,系统梳理了粘附性水凝胶的设计思路,还首次将实验性能与临床金标准进行量化对比,为口腔局部药物递送系统的合理设计,提供了全新的思路和框架。

口腔疾病困扰着全球超过35亿人,局部药物治疗一直面临诸多难题——唾液冲刷、咀嚼产生的机械压力,再加上口腔内复杂的微生物环境,都大大影响了治疗效果。传统的治疗制剂,比如含漱液、糊剂或贴片,在口腔内停留时间短,药物浓度也达不到有效治疗标准,导致疗效不理想。
针对这个临床难题,这篇论文创新地提出了“分子-网络-系统”三个层级的协同设计思路。在分子层面,研究人员参考贻贝仿生儿茶酚化学、席夫碱反应、硼酸酯键等动态共价技术,让水凝胶能在湿润的口腔表面牢牢粘附。例如,儿茶酚功能化聚丙烯酸/聚乙烯亚胺体系通过拓扑缠结,在口腔黏膜上的粘附强度能达到6到7千帕,比传统纤维素类唾液替代品不足1千帕的粘附力强得多。在网络层面,研究采用双网络、互穿网络以及抗溶胀结构,来增强水凝胶的韧性和抗疲劳能力。而在系统层面,通过整合Janus非对称结构、仿生微拓扑,以及能响应环境变化的模块,让水凝胶能主动感知口腔的病理环境,需要释放药物时就精准释放。
这篇论文的另一大亮点,是系统对比了各类粘附性水凝胶与传统临床制剂的性能差异,为评估该领域的研究进展提供了量化参考标准。在牙周炎治疗中,光固化HSC水凝胶在黏膜上的滞留时间可达120小时,而商业氯己定凝胶仅能停留0.5小时,且前者对牙槽骨的保留效果明显优于空白对照;在龋病防治方面,黑磷@CP5水凝胶在牙釉质上24小时的保留率达53.5%,杀菌率超过97%,传统氟化物清漆的保留率仅为19%,且前者再生的矿物层硬度接近健康牙釉质。在口腔溃疡治疗中,温敏PolyLA-SQBA水凝胶8天愈合率达93.03%,远超商业壳聚糖贴片的78.4%;针对口腔癌前病变,PACA光动力治疗贴片10秒内即可达到62千帕的粘附强度,动物模型显示,14周后其肿瘤体积仅为传统ALA溶液组的七分之一,患者满意度也显著提高。
本研究在总结现有研究成果的同时,也明确指出了当前该领域面临的诸多挑战。不同口腔部位的力学环境差异很大,比如颊黏膜与舌下区承受的剪切力、唾液冲刷强度完全不同,但现有水凝胶大多没有针对特定区域进行适配设计,难以实现全口腔范围的稳定粘附。此外,大多数研究只观察了7到14天的短期效果,可人体口腔组织真正愈合,通常需要3到4周,缺少长期的生物安全性评估,这也严重影响了水凝胶真正走进临床、投入使用。
从生产角度来说,因为加入了多层结构和智能响应模块,水凝胶的制备工艺变得比较复杂,不同批次的产品稳定性也不好,大规模生产的成本也偏高,这也限制了它的推广使用。针对这些难题,本研究提出了未来的发展方向:重点研发集成化的多因素生物反应器,能模拟出口腔里唾液流动、咀嚼疲劳以及生物膜侵袭等真实生理环境;同时推进3D/4D打印技术,让水凝胶能根据每个人的情况定制,还要建立统一的性能评价标准。研究人员表示,只要做好这些方面,粘附性水凝胶就有望摆脱单纯的药物载体身份,变成能主动响应口腔环境的智能材料,进而推动口腔疾病治疗实现质的飞跃。
罗静团队在《Diabetologia》发表糖尿病视网膜病变新成果
近日,中南大学湘雅二医院眼科罗静教授团队联合深圳眼科医院Xiaohe Yan教授团队以及山西白求恩医院雷和田教授团队,在糖尿病领域顶级期刊《Diabetologia》(中科院1区TOP,IF=10.2)在线发表题为“A diabetes-induced change of MDM2 SNP309T→G contributes to aberrant retinal angiogenesis”的原创性研究成果,首次揭示MDM2基因多态性驱动病理性视网膜血管生成的分子机制,为增殖性糖尿病视网膜病变(Proliferative diabetic retinopathy,PDR)的精准防治提供了全新策略。

糖尿病视网膜病变是工作年龄人群首位致盲眼病,其中增殖性糖尿病视网膜病变因视网膜新生血管破裂出血、牵拉视网膜脱离,致盲风险极高。临床中常观察到异质性表现:部分患者长期高血糖却未出现PDR,而部分患者短期内即进展为重症,遗传差异被认为是关键诱因之一。MDM2作为调控p53的核心负反馈蛋白,其第二启动子区的SNP309T→G突变已被证实与癌症、增殖性玻璃体视网膜病变(Proliferative vitreoretinopathy,PVR)密切相关,但该突变是否参与PDR发生及其具体机制尚未明确。
该研究首先通过临床样本验证遗传变异特征,收集110例PDR患者纤维血管膜(Fibrovascular membranes,FVMs)与外周血配对样本,发现60.1%的患者FVMs中存在MDM2 SNP309G等位基因,远高于外周血的20.9%;其中20.9%的患者FVMs中出现T→G突变,与自身外周血基因型不一致,而对照组PVR患者未见此现象,提示糖尿病眼内微环境可特异性诱导MDM2基因突变。进一步机制研究显示,PDR患者玻璃体中氧化损伤标志物8-氧代-2'-脱氧鸟苷(8-oxo-dG)水平较PVR对照组升高7.8倍,长期暴露于此环境的人视网膜微血管内皮细胞中,36.1%发生MDM2 SNP309T→G突变,伴随MDM2表达升高、抑癌蛋白p53降解。团队利用前沿的先导编辑(prime editing)技术构建MDM2 SNP309G细胞模型,证实该突变可显著增强内皮细胞增殖、迁移与成管能力,进一步放大高糖诱导的血管生成效应。
在动物层面,研究采用携带MDM2 SNP309T/T或G/G等位基因的小鼠构建氧诱导视网膜病变模型,发现携带SNP309G的小鼠视网膜病理新生血管面积较野生型增加2.3倍,分子机制解析显示其通过“MDM2↑→HIF-1α↑→VEGF↑→VEGFR2/ERK1/2/Sp1磷酸化↑→MDM2进一步上调”的正反馈环路,持续驱动血管异常增生。
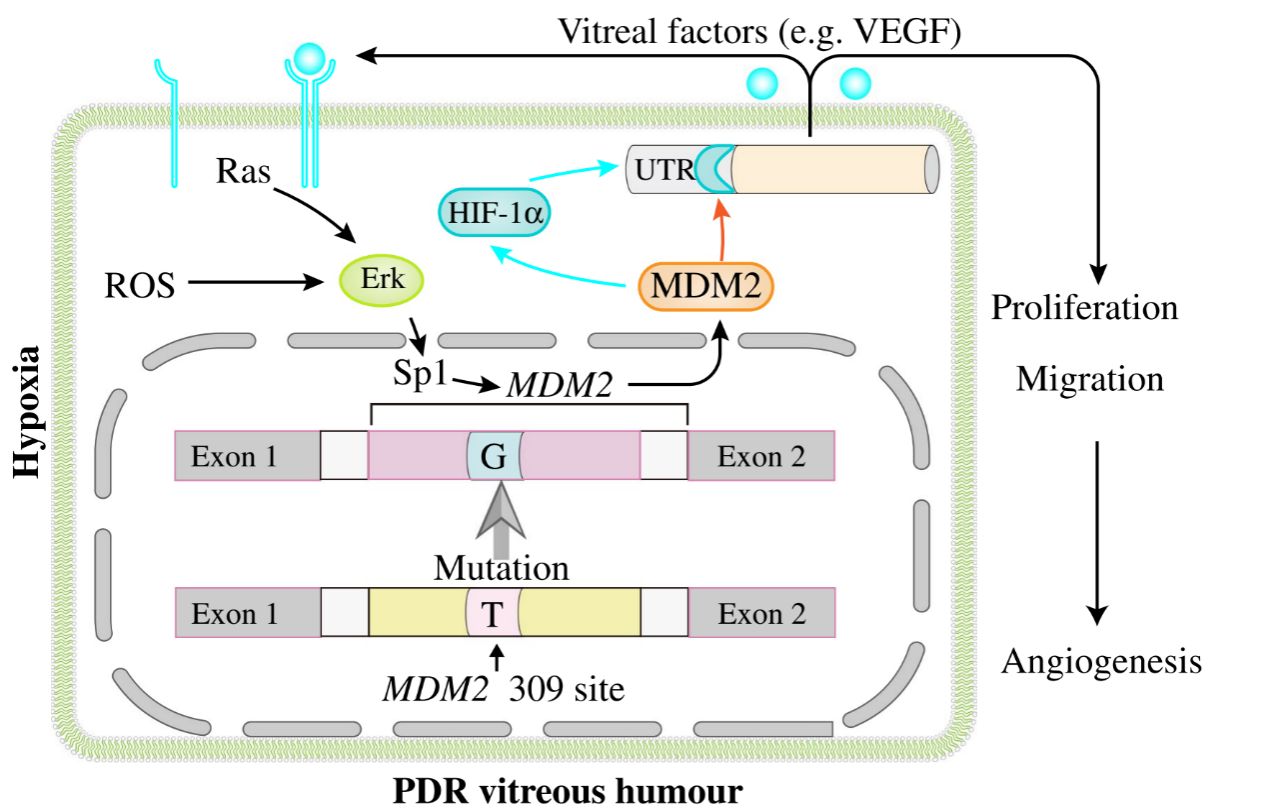
该研究突破了既往仅靶向VEGF的单一干预思路,首次提出靶向MDM2第二启动子、阻断上述正反馈环路,有望从源头抑制病理性血管生成,为PDR患者提供更长效的治疗选择。
原文链接:https://doi.org/10.1007/s00125-026-06695-5。
陈世杰、李劲松团队在《Bioactive Materials》发表研究成果
近日,中南大学湘雅三医院脊柱外科陈世杰教授、李劲松副教授团队在国际权威学术期刊《Bioactive Materials》(生物活性材料,中科院一区,Top期刊,影响因子20.3)发表题为 “Manganese-potentiated cGAS–STING activation with ATM/PRMT5 inhibition remodels the immunosuppressive microenvironment in osteosarcoma via bone-targeted delivery”(锰增强的cGAS-STING激活联合ATM/PRMT5抑制,通过骨靶向递送重塑骨肉瘤中的免疫抑制微环境)的原创研究论文。
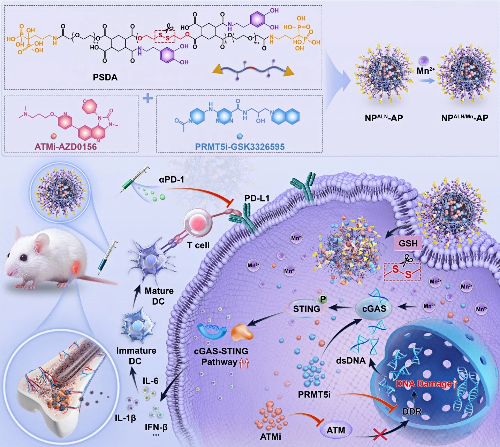
研究发现,ATM和PRMT5在骨肉瘤组织中高表达,并与DNA损伤修复相关通路密切相关。双重抑制ATM和PRMT5可显著加重骨肉瘤细胞DNA损伤,促进胞质双链DNA积累,并进一步激活cGAS-STING先天免疫通路。在此基础上,NPALN/Mn-AP可在骨肉瘤病灶中实现较好的富集与滞留,并在体内外实验中表现出明显的抗肿瘤作用和良好的生物安全性。进一步研究显示,NPALN/Mn-AP不仅能够直接增强骨肉瘤细胞损伤,还可通过激活cGAS-STING通路改善肿瘤免疫微环境,促进树突状细胞成熟、增强CD8⁺T细胞活化与浸润,并减少免疫抑制性细胞积累。联合αPD-1治疗后,其抗肿瘤效果进一步增强。该研究将骨靶向纳米递送、ATM/PRMT5双重DNA损伤修复抑制和Mn²⁺增强先天免疫激活整合于同一治疗体系,为骨肉瘤纳米免疫治疗提供了新的策略参考。
余正团队发表肠道微生物氨调控肠动力的原创成果
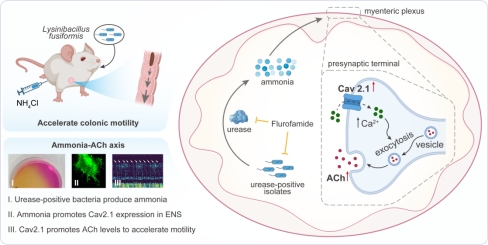
近日,国际微生物领域顶级期刊《Nature Microbiology》(IF=20.4)以Research Briefing形式专题报道中南大学湘雅基础医学院人体微生物与健康课题组余正团队研究成果“Gut bacteria ammonia production restores acetylcholine neurotransmission and bowel motility”,同步刊发专家评述与编辑推荐,标志我国学者在肠道菌群——肠神经系统交叉领域获重要突破。
在这项研究中,余正团队提出了一种新的宿主-菌群互作框架,当肠动力受损、胆碱能信号减弱时,肠道菌群并非被动变化,而是可通过增强脲酶活性和氨生成,对宿主神经递质不足作出代偿性响应,从而帮助维持肠道运动功能。这一发现提示,肠道微生物来源的氨并非单纯有害副产物,而是可增强肠神经兴奋性、恢复胆碱能神经传递并维持肠道蠕动的功能性信号。本研究深化了对“肠道菌群-肠神经系统”互作的理解,为肠动力障碍提供了全新的干预思路。通过将微生物氮代谢与神经递质调控直接连接起来,拓展了微生物代谢在维持宿主生理稳态中的功能边界。
周文虎、刘俊彦团队在《Acta Pharmaceutica Sinica B》发表骨关节炎靶向治疗最新研究成果
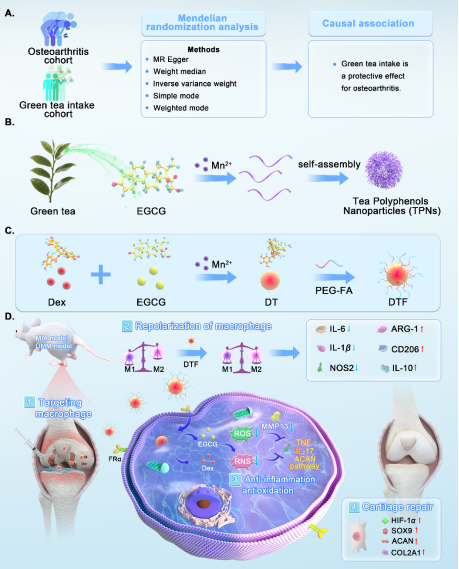
近日,中南大学湘雅药学院周文虎教授团队与湘雅三医院刘俊彦副研究员团队合作,在国际药学领域权威期刊Acta Pharmaceutica Sinica B(IF=15.2)上发表了关于骨关节炎治疗的最新研究成果。该研究创新性地提出了“遗传证据引导的纳米治疗”新策略,成功探索了一条从人群宏观证据到靶向药物设计的转化路径,为突破骨关节炎(OA)临床治疗瓶颈提供了富有前景的新方向。
研究团队开创性地将人类遗传学证据与纳米药物设计相结合,提出全新研发策略。通过对超过47万人的遗传数据进行孟德尔随机化分析,研究首次在因果关联层面证实了“饮用绿茶可降低OA风险”。这一关键发现,将绿茶中的核心活性成分——表没食子儿茶素没食子酸酯及其自组装形成的茶多酚纳米颗粒,确立为极具潜力的治疗候选“基石”。
基于此发现,联合研究团队成功构建了一种多功能纳米治疗平台(DTF)。该平台以生物相容性优异的天然茶多酚纳米颗粒为载体,高效负载临床抗炎药地塞米松,并通过表面修饰的叶酸分子,实现对OA关节中高表达叶酸受体-β的滑膜巨噬细胞的精准靶向。
原文链接:https://www.sciencedirect.com/science/article/pii/S2211383526001681
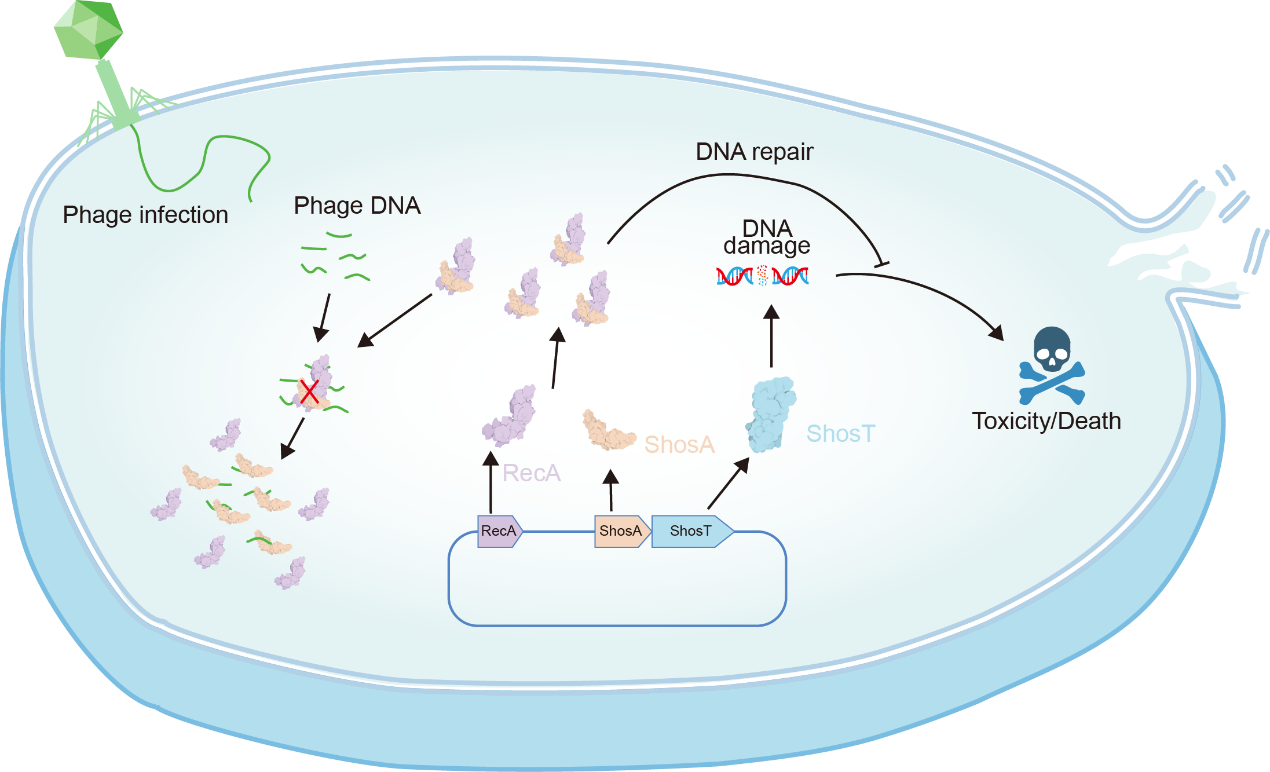
李发祥课题组研究揭示细菌抗噬菌体防御的分子机制
近日,中南大学李发祥课题组在国际知名期刊《核酸研究》(Nucleic Acids Research)(IF=16.8)发表题为“ShosTA系统介导抗噬菌体防御的分子机制(The molecular mechanisms of the ShosTA system in mediating anti-phage defense)”的原创性学术论文。该工作从结构生物学视角,深入阐明了细菌毒素-抗毒素(TA)系统ShosTA感知入侵噬菌体DNA信号并触发“流产感染”(abortive infection)的底层逻辑;揭示了被感染细胞如何通过“自杀”机制遏制噬菌体扩增,从而保全整个细菌种群的分子过程。本研究不仅完善了细菌的免疫防御网络模型,也为开发针对耐药菌的噬菌体疗法,以及设计靶向抗毒素蛋白的新型抗菌小分子拮抗剂提供了坚实的理论基础。